17.1.8. Реакции с α,β-ненасыщенными кетонами, нитрилами и нитросоединениями
Эти катализируемые кислотами реакции следует рассматривать как дальнейшее развитие конденсаций индолов с альдегидами и кетонами, рассмотренных в предыдущем разд. 17.1.7. В простейшем примере метилвинилкетон взаимодействует с индолом просто как сопряжённый кетон (по β-положению двойной связи) [58].
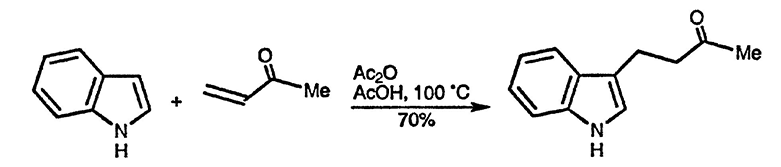
Использование монтмориллонитовой глины — очень эффективного «кислотного» катализатора — позволяет проводить α-алкилирование β-замещённых индолов [59]; трифлат иттербия также может служить катализатором таких процессов алкилирования [60]. Этому эффективному катализу можно противопоставить реакцию окиси мезитила с 1,3-диметилиндолом в присутствии серной кислоты — электрофильная атака идёт по уже замещённому β-положению с последующим внутримолекулярным нуклеофильным присоединением енольной формы кетона в боковой цепи по положению 2 [61].
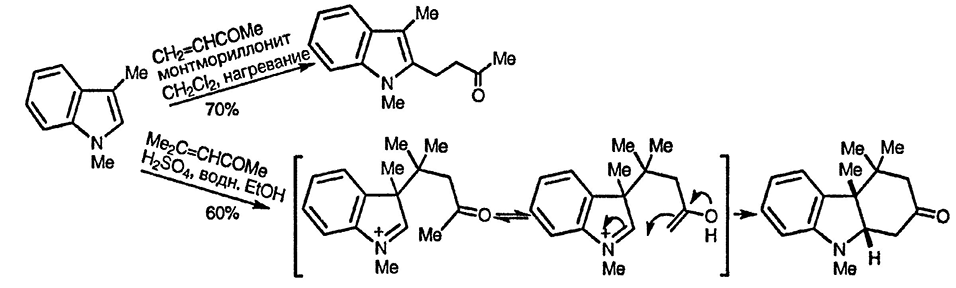
Развитие этой методологии позволило синтезировать триптофаны в результате катализируемого хлоридом алюминия алкилирования иминоакрилатом, как показано ниже [62] (подобные трансформации, но биокатализируемые, см. в разд. 2.9.):
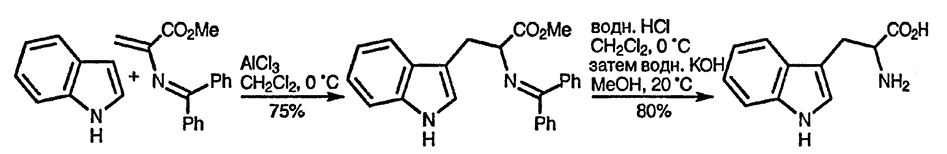
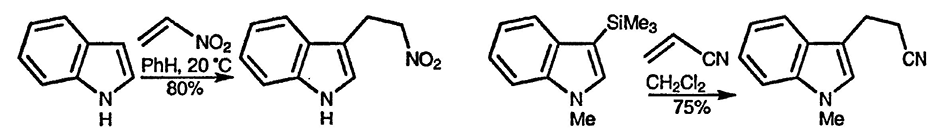
Электрофильность нитроэтена достаточна для замещения индола даже в отсутствие кислотного катализа [63]; при использовании 2-диметиламино-1-нитроэтена в трифторуксусной кислоте получают 2-(индол-3-ил)нитроэтен — реакционноспособную частицу, представляющую собой протонированный енамин, и процесс подобен конденсации Манниха [64]. Применение 3-триметилсилил-индолов с ипсо-замещением силана [65] — альтернативный метод эффективного алкилирования, позволяющий избегать кислотного катализа.
17.1.8. Реакции с α,β-ненасыщенными кетонами, нитрилами и нитросоединениями
Список литературы к главе 17
Упражнения к главе 17
Глава 17
- 17. Индолы: реакции и методы синтеза
- 17.1. Реакции с электрофильными реагентами
- 17.1.1. Протонирование
- 17.1.2. Нитрование; реакции с другими азотсодержащими электрофилами
- 17.1.3. Сульфирование; реакции с другими серосодержащими электрофилами
- 17.1.4. Галогенирование
- 17.1.5. Ацилирование
- 17.1.6. Алкилирование
- 17.1.7. Реакции с альдегидами и кетонами
- 17.1.8. Реакции с α,β-ненасыщенными кетонами, нитрилами и нитросоединениями
- 17.1.9. Реакции с иминиевыми ионами: реакция Манниха
- 17.1.10. Диазосочетание и нитрозирование
- 17.1.11. Электрофильное металлирование
- 17.1.11.1. Меркурирование
- 17.1.11.2. Таллирование
- 17.1.11.3. Палладирование
- 17.2. Реакции с окислителями
- 17.3. Реакции с нуклеофильными реагентами
- 17.4. Реакции с основаниями
- 17.4.1. Депротонирование N-водорода
- 17.4.2. Депротонирование C-водорода
- 17.5. Реакции N-металлированных индолов
- 17.6. Реакции C-металлированных индолов
- 17.6.1. Литийорганические производные
- 17.6.2. Реакции, катализируемые палладием
- 17.7. Реакции со свободными радикалами
- 17.8. Реакции с восстановителями
- 17.9. Реакции с карбенами
- 17.10. Электроциклические и фотохимические реакции
- 17.11. Алкилиндолы
- 17.12. Реакции C-замещённых индольных соединений
- 17.13. Индолкарбоновые кислоты
- 17.14. Гидроксииндолы
- 17.14.1. Оксиндол
- 17.14.2. Индоксил
- 17.14.3. Изатин
- 17.14.4. 1-Гидроксиндол
- 17.15. Аминоиндолы
- 17.16. Азаиндолы
- 17.16.1. Реакции электрофильного замещения
- 17.16.2. Реакции нуклеофильного замещения
- 17.17. Синтезы индолов
- 17.17.1. Синтезы кольца
- 17.17.1.1. Из фенилгидразонов альдегидов и кетонов
- 17.17.1.2. Из o-(2-оксоалкил)анилинов
- 17.17.1.3. Из o-алкинилариламинов
- 17.17.1.4. Из o-толуидинов
- 17.17.1.5. Из α-ариламинокарбонильных соединений
- 17.17.1.6. Синтез из пирролов
- 17.17.1.7. Из орто-замещённых нитроаренов
- 17.17.1.8. Из N-ариленаминов
- 17.17.1.9. Из N-аллил-o-галогенариламинов
- 17.17.1.10. Из енаминов и п-хинонов
- 17.17.1.11. Из ариламинов
- 17.17.1.12. Из o-ациланилидов
- 17.17.1.13. Из o-изоцианостиролов
- 17.17.1.14. Из o-хлорацетилариламинов
- 17.17.1.15. Циклизацией нитренов
- 17.17.1.16. Циклизации аринов
- 17.17.1.17. Из o-нитростиролов
- 17.17.1.18. Из индолинов
- 17.17.2. Синтезы оксиндолов
- 17.17.3. Синтезы индоксилов
- 17.17.4. Синтез изатинов
- 17.17.5. Синтезы 1-гидроксиндолов
- 17.17.6. Примеры синтезов некоторых важных производных индола
- 17.17.6.1. Ондансетрон
- 17.17.6.2. Стауроспорин агликон
- 17.17.6.3. Серотонин
- 17.17.6.4. Хуангксинмицин
- 17.17.7. Синтезы азаиндолов
Дополнительно:
В монографии впервые в мировой литературе систематизирован и обобщён обширный ...
 Химические волокна. Словарь-справочник
Химические волокна. Словарь-справочник В словаре приводятся в алфавитном порядке русские и иностранные торговые и ...
 Окислительно-восстановительные полимеры (редокс-полимеры)
Окислительно-восстановительные полимеры (редокс-полимеры) Книга является первой монографией об окислительно-восстановительных полимерах, ...