26.3. Бензотриазолы
Химия бензотриазола изучена подробно и в настоящее время находит широкое применение для гетероциклических [131] и общих синтезов [132]. Это обусловлено целым рядом полезных свойств бензотриазола: (1) α-карбанионы стабилизированы точно так же, как бензильное положение бензольных структур; (2) α-карбокатионы также стабилизированы; (3) бензотриазолил-анион представляет собой хорошую уходящую группу в сочетании с высокой реакционной способностью и стабильностью и поэтому удобен в применении. Последовательные комбинации свойств позволяют применять его для синтеза широкого круга соединений — некоторые примеры представлены ниже.
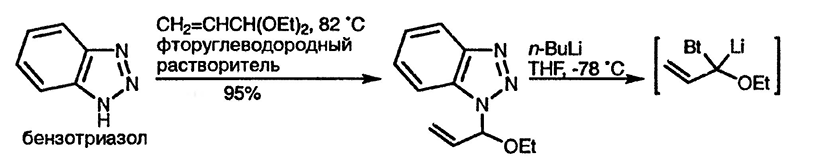
Исходные производные бензотриазола обычно получают из незамещённого гетероцикла N-алкилированием алкилгалогенидом или реакцией с альдегидами или ацеталями, в результате чего образуется смесь 1- и 2-замещённых бензотриазолов, однако реакционная способность этих двух изомеров одинакова. Для ясности приведены реакции только для 1-замещённых соединений.
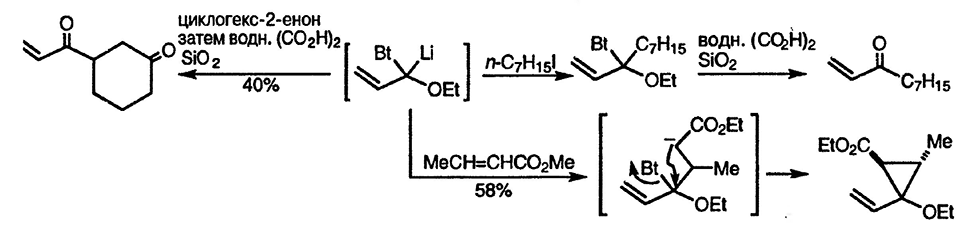
Алкилирование литиированного 1-(1-этоксипроп-2-енил)бензотриазола приводит к образованию енонов после гидролитического удаления гетероцикла; присоединение литиевых производных к циклогексанону даёт 1,4-дикетон, как показано ниже на схеме [133]. При присоединении подобного аниона к метил-кротонату образуется анион, в котором происходит внутримолекулярное замещение бензотриазола и получается циклопропан [134].
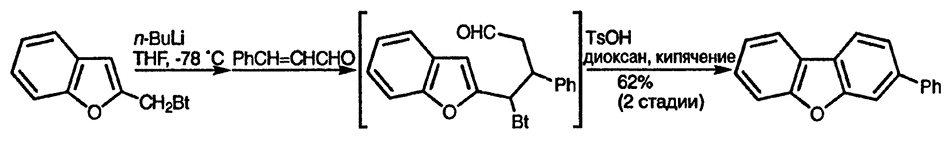
В приведённом ниже примере бензотриазольный фрагмент облегчает литиирование по бензильному положению и на последней стадии выступает в качестве уходящей группы [135].
Способность бензотриазола стабилизировать катион позволяет 1-гидрокси-метилбензотриазину алкилировать индол; образующееся соединение затем литиируют, что даёт возможность проводить электрофильное замещение, и далее бензотриазольный фрагмент замещается реактивом Гриньяра [136]
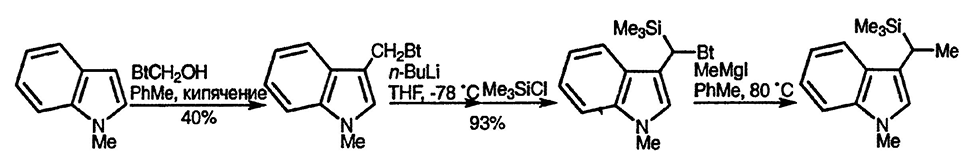
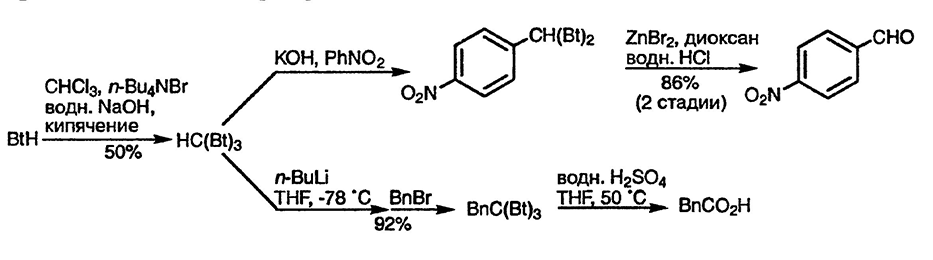
Анион трис(бензотриазол-1-ил)метана может присоединяться к нитробензолу по механизму викариозного нуклеофильного замещения, при котором бензотриазольный фрагмент служит одновременно для стабилизации аниона и как уходящая группа [137]; другое применение этого соединения продемонстрировано на примере алкилирования его аниона с последующим гидролизом и превращением в кислоту [138].
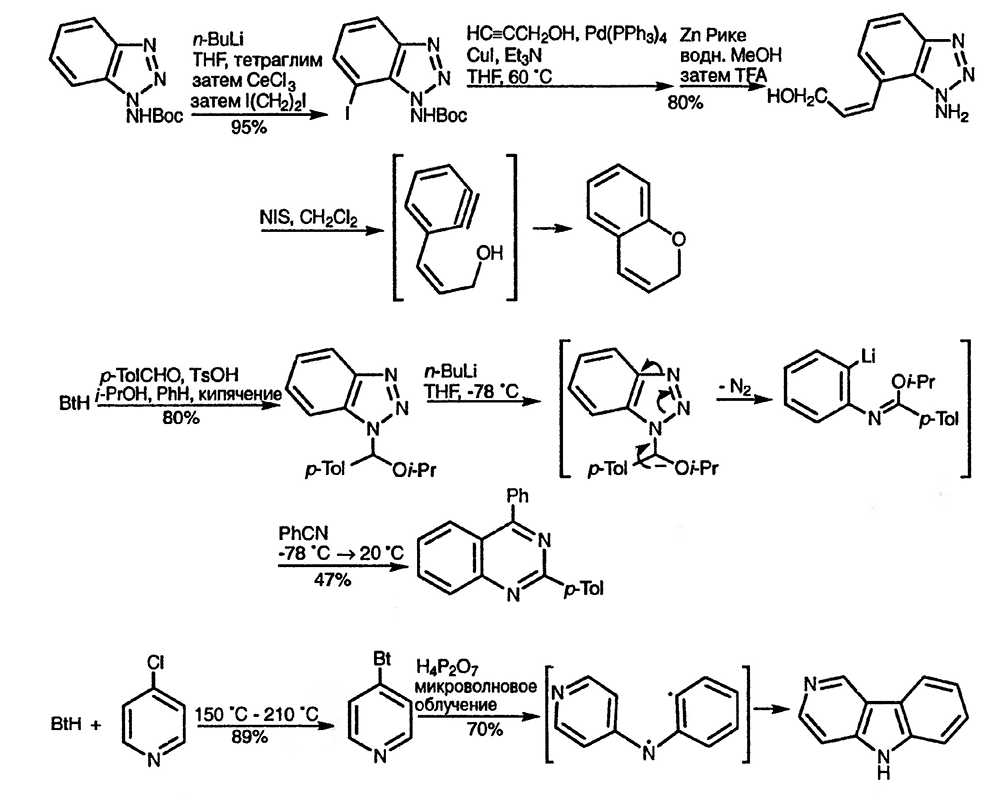
Реакционная способность бензотриазолов позволяет их использовать для получения других гетероциклических соединений в результате разнообразных реакций, приводящих к раскрытию цикла и образованию реакционноспособных интермедиатов, таких, как дегидробензолы [139], ариллитиевые производные [140] и бирадикалы, как показано ниже [141]:
Глава 26
- 26. Гетероциклы, содержащие более двух гетероатомов
- 26.1. Пятичленные циклы
- 26.1.1. Азолы
- 26.1.1.1. 1,2,3-Триазол
- 26.1.1.2. 1,2,4-Триазол
- 26.1.1.3. Тетразол
- 26.1.1.4. Синтез циклической системы азолов
- 26.1.2. Оксадиазолы и тиадиазолы
- 26.1.3. Другие системы
- 26.1.4. Синтезы кольца
- 26.1.4.1. 1,2,4-Оксадиазолы
- 26.1.4.2. 1,3,4-Оксадиазолы
- 26.1.4.3. 1,2,5-Оксадиазолы
- 26.1.4.4. Сидноны
- 26.1.4.5. 1,2,3-Тиадиазолы
- 26.1.4.6. 1,2,4-Тиадиазолы
- 26.1.4.7. 1,3,4-Тиадиазолы
- 26.1.4.8. 1,2,5-Тиадиазолы
- 26.2. Шестичленные циклы
- 26.2.1. Азины
- 26.2.2. Синтезы кольца
- 26.2.2.1. 1,2,3-Триазин
- 26.2.2.2. 1,2,4-Триазины
- 26.2.2.3. 1,3,5-Триазины
- 26.2.2.4. 1,2,4,5-Тетразины
- 26.3. Бензотриазолы
Дополнительно:
В книге излагаются теоретические основы метода электрофореза на бумаге и способы ...
В книге изложены современные теоретические представления об основных процессах ...

