10. Общая характеристика реакционной способности диазинов: пиридазин, пиримидин и пиразин
Диазины — пиридазин, пиримидин и пиразин — представляют собой гетероциклические соединения, содержащие два иминных атома азота, и, следовательно, все свойства, присущие пиридину (гл. 5.), в ещё большей степени проявляются у этих гетероциклических соединений.
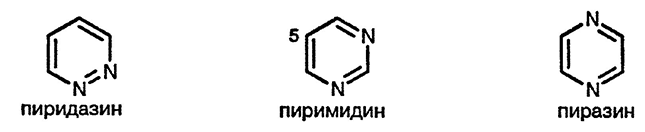
Два гетероатома оттягивают электронную плотность от атомов углерода, включённых в цикл, ещё в большей степени, чем в пиридине. Вследствие этого незамещённые диазины ещё менее склонны к реакциям электрофильного замещения, чем пиридин. Понижение электронной плотности на атомах углерода гетероциклов закономерно приводит к облегчению атаки диазинов нуклеофильными реагентами по сравнению с пиридином. Диазины в меньшей степени, чем пиридин, проявляют свойства оснований, поскольку сказывается дестабилизирующее влияние второго атома азота на катион диазиния. Тем не менее, диазины образуют соответствующие соли при реакции с алкилгалогенидами и при взаимодействии с надкислотами превращаются в соответствующие N-оксиды. Электрофильное присоединение вдет только по одному атому азота, поскольку возникающий при этом положительный заряд значительно понижает нуклеофильные свойства второго атома азота.
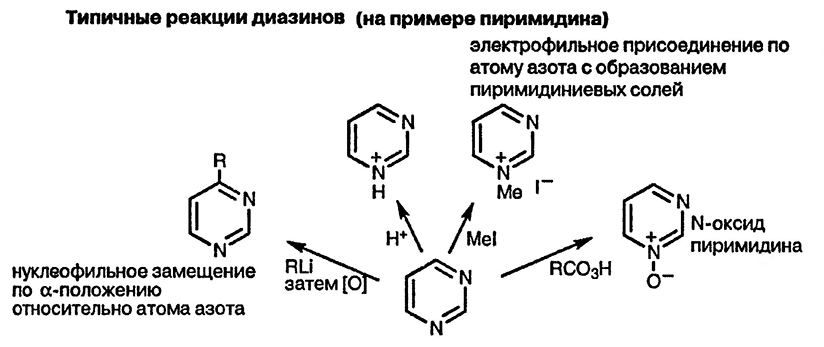
Главная особенность химических свойств диазинов связана с их электронодефицитной природой, которая определяет лёгкость присоединения нуклеофильных реагентов к гетероциклу. В отсутствие галогенидов для завершения процесса замещения необходимо окисление первоначально образующихся аддуктов. Галогенопроизводные диазинов, содержащие атомы галогена в α- или β-положении относительно атома азота, чрезвычайно легко вступают в реакции нуклеофильного замещения, поскольку интермедиаты таких процессов значительно стабилизированы.
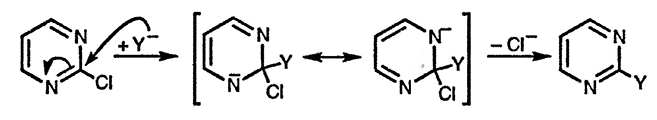
Все атомы углерода во всех диазинах, за исключением атома C(5) пиримидина, расположены в α- и/или в γ-положениях относительно иминного атома азота; кроме того, следует учитывать, что наличие дополнительного электроноакцепторного атома азота повышает способность этих положений к реакциям нуклеофильного присоединения/замещения. Поэтому все моногалогенопроизводные диазинов более склонны к реакциям с нуклеофилами, чем 2- или 4-гало-генопиридины. 2- и 4-Галогенопиримидины обладают наибольшей реакционной способностью, поскольку образующиеся в ходе процесса анионные интермедиаты (показано ниже на примере 2-хлорпиримидина) мезомерно стабилизированы одновременно двумя атомами азота.
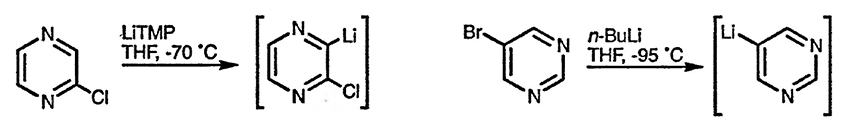
Несмотря на особенную склонность диазинов к реакциям нуклеофильного присоединения, С-литиирование диазинов можно осуществить в результате либо обмена металл — галоген, либо депротонирования по положению, соседнему с хлор- или алкоксизаместителем, однако такие процессы необходимо проводить при очень низкой температуре, чтобы избежать нуклеофильного присоединения литийорганических соединений.
Одновременно с высокой склонностью к реакциям нуклеофильного присоединения диазины легко вступают в реакции радикального замещения Минисци. Для получения различных производных диазинов широко используются реакции сочетания, катализируемые соединениями палладия(0); один пример такой реакции приведён ниже (детально такие процессы обсуждены в разд. 2.7.):
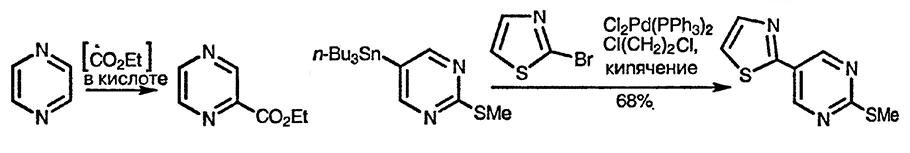
Дальнейшие аналогии с химическими свойствами пиридина, связанные с наличием электронодефицитного иминного фрагмента, проявляются в стабильности диазинов к окислительному расщеплению и в то же время в склонности к лёгкому восстановлению.
Хотя количественная мера ароматичности соединений всегда служит предметом дебатов, диазины, как принято считать, менее резонансно стабилизированы, чем пиридины, то есть они «менее ароматичны». Так, для всех диазинов известны примеры реакции Дильса-Альдера, в которых они принимают участие в качестве диенов. Первоначально образующиеся аддукты теряют малую молекулу, в случае пиримидина — циановодород, и превращаются в стабильные соединения.
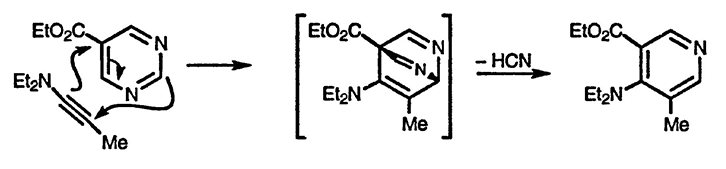
N-Оксиды диазинов, так же как и N-оксиды пиридинов, проявляют повышенную по сравнению с самими диазинами склонность к реакциям нуклеофильного и электрофильного замещения. На приведённой ниже схеме показана последовательность превращения N-оксида пиридазина, в которой на первой стадии происходит электрофильное нитрование, а на второй — нуклеофильное замещение с удалением нитрит-иона.
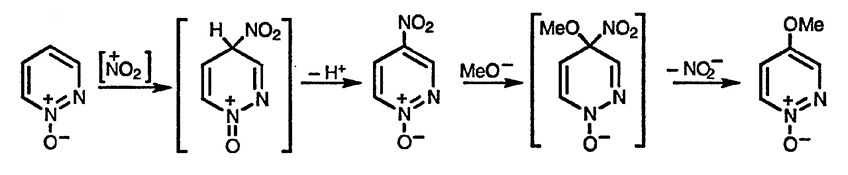
N-Оксиды диазинов обеспечивают широкие синтетические возможности для получения различных производных шестичленных гетероциклических соединений. Одна из таких полезных реакций связана с введением атома хлора в α-положение к атому азота при взаимодействии N-оксидов с галогенидами фосфора или серы. Такое превращение осуществляется в результате первоначальной атаки атома кислорода N-оксида по атому фосфора или серы. Эта реакция имеет очень большое значение, поскольку незамещённые диазины в результате двух последовательных стадий можно превратить в хлорпроизводные, которые используются в реакциях нуклеофильного замещения.
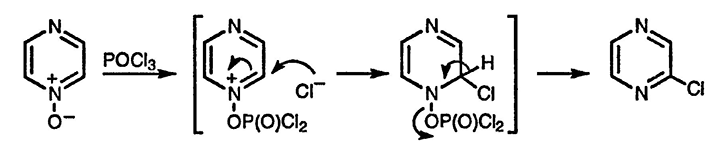
Наиболее широко изучены окси- и аминопроизводные пиримидинов, так как урацил, тимин и цитозин обнаружены в качестве оснований в ДНК и РНК. Поскольку двойная связь в таких производных диазинов с двумя кислородными заместителями аналогична енамидной двойной связи, электрофильное замещение в таких соединениях значительно облегчено; так, например, урацил можно превратить в соответствующее бромпроизводное. Присутствия одного аминного заместителя достаточно для активирования диазинового цикла к реакциям электрофильного замещения, а при наличии двух аминных или одного аминного и одного кислородного заместителя становятся возможными реакции даже со слабыми электрофильными агентами.
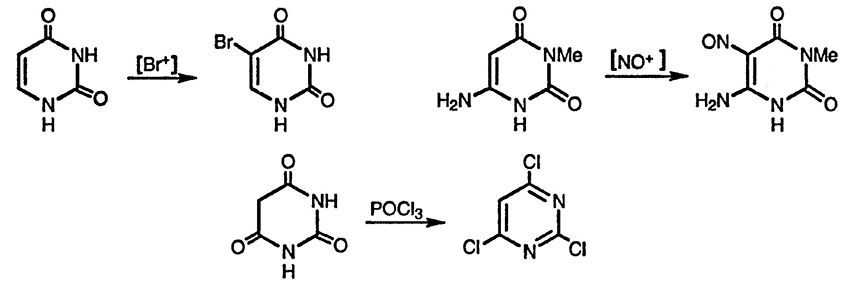
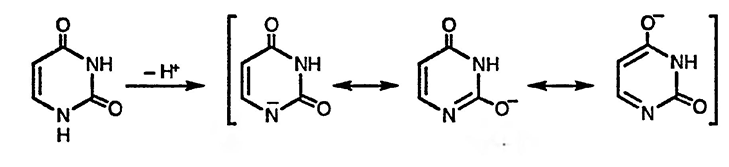
Диазиноны, аналогично пиридонам, при взаимодействии с галогенвдами фосфора превращаются в соответствующие хлорпроизводные. Образующиеся при депротонировании атома азота анионы амбидентны, и, хотя резонансные формы, аналогичные фенолят-ионам, вносят вклад в структуру таких анионов, их реакции с электрофильными алкилируюгцими агентами проходят преимущественно по атому азота.
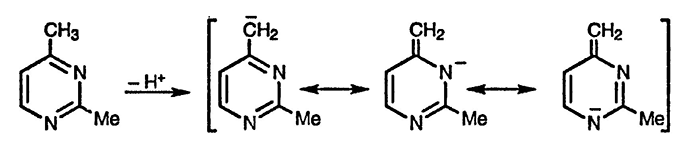
Алкильные заместители в диазиновом цикле, за исключением алкильных групп в положении 5, способны вступать в реакцию конденсации с предварительным генерированием соответствующих анионов в результате депротонирования. Как и в случае алкилпиридинов, образование таких анионов становится возможным вследствие делокализации отрицательного заряда с участием одного или двух атомов азота цикла.
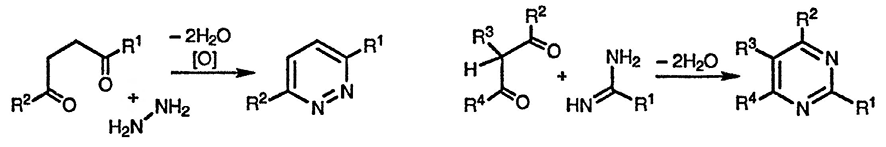
Как показано ниже, любой диазин можно получить в результате комбинирования молекулы, содержащей два атома азота, с молекулой дикарбонильного соединения. В случае пиридазина источником атомов азота, очевидно, служит гидразин, который при взаимодействии с 1,4-дикарбонильными соединениями образует дигидропиридазины, легко дегидрируемые в соответствующие ароматические соединения. Производные пиримидина получаются при реакции 1,3-дикарбонильных соединений с амидином (пример приведён на схеме), мочевиной (при этом образуется 2-пиримидон) или гуанидином (используется для получения 2-аминопиримидинов), причём в этом случае нет необходимости в стадии окисления.
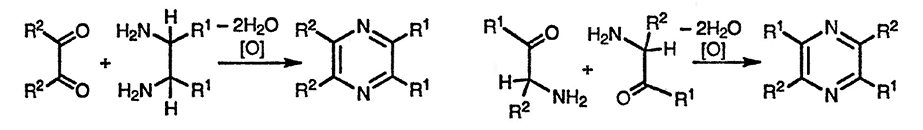
Синтез пиразинов требует комбинации молекулы 1,2-диамина с молекулой 1,2-дикарбонильного соединения и последующего окисления, однако, если каждая из комбинируемых молекул несимметрична, образуется смесь продуктов циклизации. Димеризация 2-аминокарбонильных соединений также приводит к образованию симметрично замещённых пиразинов. Наиболее хорошо известный пример такого превращения связан с димеризацией природных аминокислот и их эфиров, приводящей к образованию дигидропиразин-2,5-дионов — «дикетопиперазинов».
10. Общая характеристика реакционной способности диазинов: пиридазин, пиримидин и пиразин
Глава 10
- 10. Общая характеристика реакционной способности диазинов: пиридазин, пиримидин и пиразин
Дополнительно:
 Строение стекла
Строение стекла Москва — Ленинград, 1955 год. Издание Академии наук СССР. Издательский переплёт. ...
 Магний
Магний High Quality Content by WIKIPEDIA articles! Ма?гний — элемент главной подгруппы второй группы, ...
 Справочник по охране труда и технике безопасности в химической промышленности. Новые и пересмотренные правила и инструкции по устройству и эксплуатации оборудования и по промышленной санитарии
Справочник по охране труда и технике безопасности в химической промышленности. Новые и пересмотренные правила и инструкции по устройству и эксплуатации оборудования и по промышленной санитарии Справочник содержит в систематизированном виде официальные и ведомственные ...
