11. Диазины, пиридазины, пиримидины и пиразины: реакции и методы синтеза
Все три диазина — пиридазин [1], пиримидин [2] и пиразин [3] — представляют собой устойчивые бесцветные соединения, растворимые в воде. Незамещённые диазины, в отличие от пиридина, трудно доступны и дороги, вследствие чего, редко используются в качестве исходных соединений для получения производных диазинов. Аннелирование бензольного кольца к диазиновому возможно лишь четырьмя способами, и существует лишь четыре бензодиазина: циннолин, фталазин, хиназолин и хиноксалин.
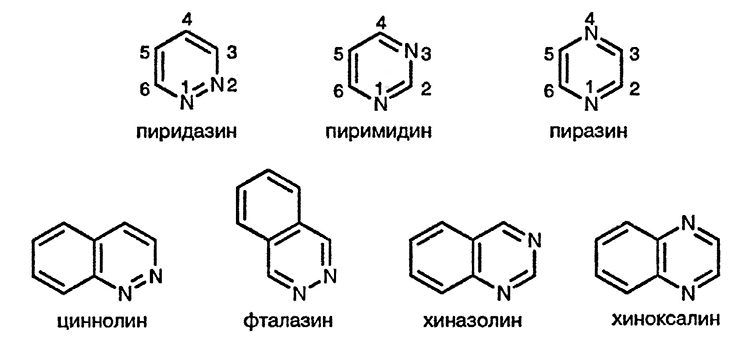
Пиридазин отличается от других диазинов поразительно высокой температурой кипения (207 °C), что на 80–90 °C выше температур кипения пиримидина (123 °C), пиразина (118 °C) и других азинов, включая 1,3,5-триазины, температуры кипения которых лежат в интервале 114-124 °C. Такая высокая температура кипения пиридазина связана со способностью связи N—N к поляризации, что обеспечивает высокую степень диполярной ассоциации молекул в жидкости.
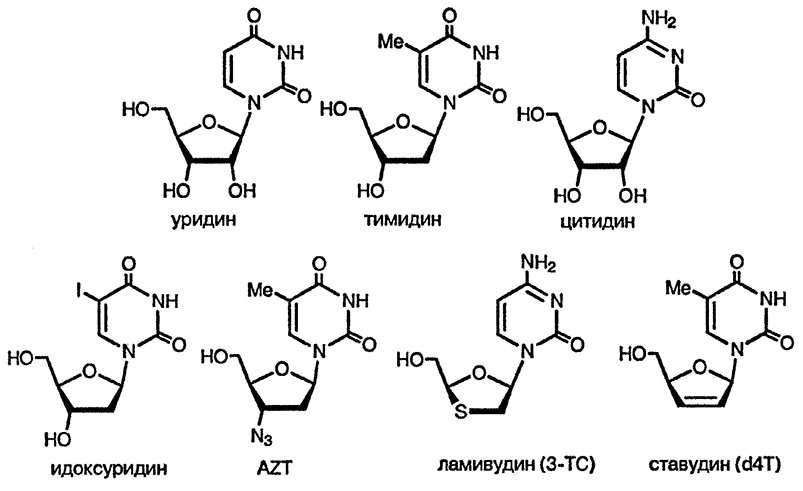
Наиболее важные встречающиеся в природе диазины — это пиримидиновые основания: урацил, тимин и цитозин, которые входят в состав нуклеиновых кислот [4]. Среди некоторых аналогов пиримидиновых нуклеозидов были обнаружены антивирусные агенты, такие, как идоксуридин, применяемый для лечения глазных заболеваний, вызванных вирусом Herpes, AZT — препарат, наиболее часто используемый для лечения ВИЧ, ламивудин (3-ТС), используемый одновременно для лечения гепатита В и ВИЧ-инфекций, и ещё один препарат против ВИЧ-инфекций — ставудин (d4T). Пиримидиновый фрагмент содержится также в молекуле тиамина (витамин B1) (разд. 21.11.). Часто пиримидиновые циклы в нуклеиновых кислотах изображают иначе, чем в этой главе: при этом пиримидиновый цикл перемещают относительно горизонтальной оси таким образом, что атом N3 становится «направленным» на северо-запад. Такой приём используется главным образом для того, чтобы подчеркнуть сходство пиримидинового цикла с пуринами нуклеиновых кислот (гл. 24.), которые традиционно представляют таким образом, чтобы пиримидиновая часть бициклической пуриновой системы была расположена слева.
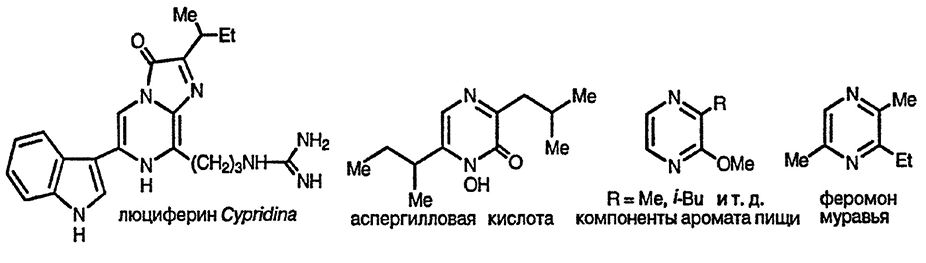
Пиразиновый цикл обнаружен в аспергилловой кислоте — метаболите грибов — и в дигидроформе в люциферинах некоторых жуков, в том числе и светлячков Cypridina hilgendotfii, ответственных за хемилюминесценсию [5]. Простые метоксипиразины обусловливают аромат большинства фруктов и овощей, таких, как горох и стручковый перец, и вин [6]. Даже если эти соединения присутствуют в незначительных количествах, они обладают заметным запахом и могут быть обнаружены в концентрации 0,00001 миллионных долей. Родственные соединения, образующиеся в результате пиролиза аминокислот в процессе приготовления пищи, ответственны за аромат жареного мяса. Некоторые поли-алкилпиразины — феромоны насекомых; например, 2-этил-3,6-диметилпиразин, представляет собой главный компонент феромона южноамериканского муравья-листоеда.
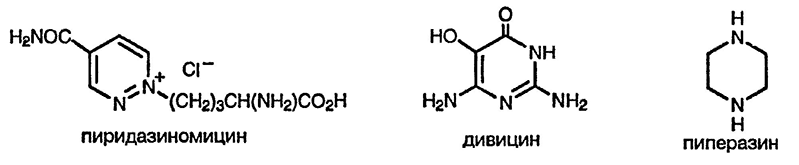
Производные пиридазинов редко встречаются в природе; среди природных соединений, содержащих пиридазиновый цикл, следует упомянуть, например, метаболиты грибов Streptomyces, содержащие главным образом восстановленный цикл, и четвертичную соль — пиридазиномицин. Дивицин, присутствующий в качестве глюкозида в конских бобах и некоторых родственных растениях, представляет собой токсин, ответственный за «фавизм» — опасную гемолитическую реакцию у генетически предрасположенных людей (обычно проживающих в Средиземноморье). Пиперазин (гексагидропиразин) используется для лечения глистной инвазии.
Производные всех трёх диазинов широко исследовались на предмет их применения в качестве синтетических лекарственных препаратов (см. также выше). К числу наиболее широко используемых для этих целей соединений диазинового ряда относятся антибактериальный препарат триметоприм, антималярийный препарат пириметамин и антигипертензивное средство гидралазин, содержащий бициклическую фталазиновую систему.
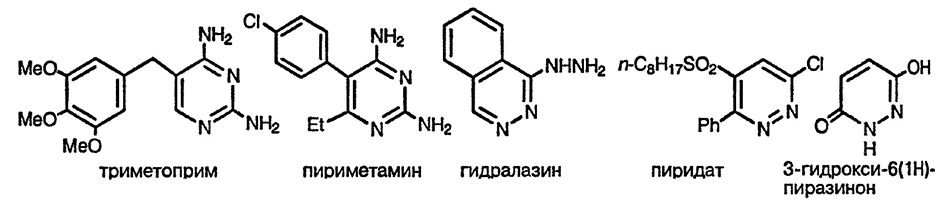
Некоторые пиридазины представляют собой селективные регуляторы роста растений и используются в качестве гербицидов: например, пиридат [3-гидрокси-6(1Н)-пиразинон] применяют для уничтожения сорняков.
11. Диазины, пиридазины, пиримидины и пиразины: реакции и методы синтеза
Список литературы к главе 11
Упражнения к главе 11
Глава 11
- 11. Диазины, пиридазины, пиримидины и пиразины: реакции и методы синтеза
- 11.1. Реакции с электрофильными реагентами
- 11.1.1. Присоединение по атому азота
- 11.1.1.1. Протонирование
- 11.1.1.2. Алкилирование
- 11.1.1.3. Окисление
- 11.1.2. Замещение при атоме углерода
- 11.1.2.1. Галогенирование
- 11.2. Реакции с окислителями
- 11.3. Реакции с нуклеофильными реагентами
- 11.3.1. Замещение атома водорода
- 11.3.1.1. Алкилирование и арилирование
- 11.3.1.2. Аминирование
- 11.3.2. Замещение других уходящих групп
- 11.4. Реакции с основаниями
- 11.4.1. Депротонирование при атоме углерода
- 11.4.2. Металлирование
- 11.5. Реакции С-металлированных диазинов
- 11.5.1. Литийорганические производные
- 11.5.2. Реакции, катализируемые палладием
- 11.6. Реакции с восстановителями
- 11.7. Реакции со свободными радикалами
- 11.8. Электроциклические реакции
- 11.9. N-оксиды диазинов
- 11.10. Оксидиазины
- 11.10.1. Строение оксидиазинов
- 11.10.2. Реакции оксидиазинов
- 11.10.2.1. Реакции с электрофильными реагентами
- 11.10.2.2. Реакции с нуклеофильными реагентами
- 11.10.2.3. Реакции с основаниями
- 11.10.2.4. Замещение атома кислорода
- 11.10.2.5. Реакции, катализируемые переходными металлами
- 11.10.2.6. Электроциклические реакции
- 11.11. Аминодиазины
- 11.12. Алкилдиазины
- 11.13. Четвертичные азиниевые соли
- 11.14. Синтез диазинов
- 11.14.1.1. Из 1,4-дикарбонильных соединений и гидразина
- 11.14.1.2. Реакцией циклоприсоединения 1,2,4,5-тетразина к производным ацетилена
- 11.14.1.3. С использованием других реакций циклоприсоединения
- 11.14.1.3.1. С использованием галогеносодержащих гидразонов
- 11.14.1.3.2. С использованием S,S-диоксидов тиофена
- 11.14.1.3.3. С использованием галогенозамещённых циклопропенов
- 11.14.2. Синтез пиримидинового кольца
- 11.14.2.1. Из 1,3-дикарбонильных соединений и соединений, содержащих фрагмент N-C-N
- 11.14.2.2. Реакцией циклоприсоединения 1,3,5-диазинов к производными ацетилена
- 11.14.2.3. Из 3-этоксиакрилоилизоцианата и первичных аминов
- 11.14.3. Синтез пиразинового цикла
- 11.14.3.1. Самоконденсацией 2-аминокетонов
- 11.14.3.2. Из 1,2-дикарбонильных соединений и 1,2-диаминов
- 11.14.3.3. Синтез пиразинов через сульфиды
- 11.14.4. Примеры некоторых важных синтезов диазинов
- 11.14.4.1. 4-Амино-5-циано-2-метилпиримидин
- 11.14.4.2. 4,6-Диамино-5-тиоформамидо-2-метилпиримидин
- 11.14.4.3. Карбоциклический бромвинилдезоксиуридин
- 11.14.4.4. Коелентеразин
- 11.14.4.5. 2,5-Диметил-3-н-пропилпиразин
- 11.15. Птеридины
Дополнительно:
 Сегнетоэлектрические твёрдые растворы на основе оксидных соединений ниобия и тантала
Сегнетоэлектрические твёрдые растворы на основе оксидных соединений ниобия и тантала В монографии изложены механизмы твердофазного взаимодействия при синтезе ...
 Каталог химических реактивов и высокочистых химических веществ
Каталог химических реактивов и высокочистых химических веществ Каталог включает около 12 тысяч наименований неорганических и органических ...
Синтез полимеров методом поликонденсации представляет значительный интерес при ...
Книга посвящена вопросам термической стабильности гетероцепных полимеров — ...