3.6. орто-Хинодиметаны в синтезе гетероциклических соединений
В последние годы существенное значение при синтезе полициклических соединений приобрели реакции, связанные с генерированием и дальнейшими превращениями орто-хинодиметанов [13]. В этом разделе приведены наиболее важные методы генерирования орто-хинодиметанов и некоторые примеры их использования. Для построения циклов наибольшее значение имеют процессы, в которых орто-хинодиметаны выступают в качестве диенов в реакциях Дильса-Альдера, приводящих, как показано ниже, к образованию ароматических циклов [14].
Хотя спектральные и некоторые другие физические свойства орто-хинодиметанов были изучены, эти соединения нестабильны, обладают высокой реакционной способностью и не могут быть выделены. Генерирование таких соединений обычно проводят в присутствии реагентов, способных взаимодействовать с ними. Аддукты орто-хинодиметанов с диоксидом серы используются для «хранения» таких соединений.
Лёгкость образования орто-хинодиметанов связана со стабильностью ароматического соединения, из производного которого они образуются, и от степени двоесвязности двух соседних атомов углерода будущего хинодиметанового фрагмента. Первый аспект можно проиллюстрировать сравнением лёгкости образования тиофен-2,3-хинодиметана [15] и аналогичного производного фурана [16]. Фурановый орто-хинодиметан гораздо более стабилен, чем соответствующее производное тиофена. Образование такого производного тиофена из ароматического тиофена требует большей затраты энергии; кроме того, реакции тиофенового производного, вновь приводящие к образованию ароматической системы, проходят значительно легче, чем в случае фуранового орто-хинодиметана.
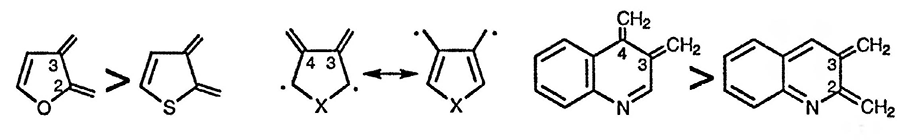
Образование орто-хинодиметанов происходит значительно легче, если степень двоесвязности орто-атомов углерода в предшественнике выше. Так, в случае пятичленных гетероароматических соединений легче образуются 2,3-хинодиметаны, а не их 3,4-аналоги. В действительности, для 3,4-хинодиметанов может быть написана резонансная структура, имеющая бирадикальный характер, и, следовательно, обладающая высокой энергией. В случае бициклических шестичленных ароматических соединений, например, хинолина [17], гораздо легче образуются 3,4-хинодиметаны, а не 2,3-аналоги. Это связано с тем, что при образовании 3,4-хинодиметанов не происходит потери в резонансной стабилизации второго цикла.
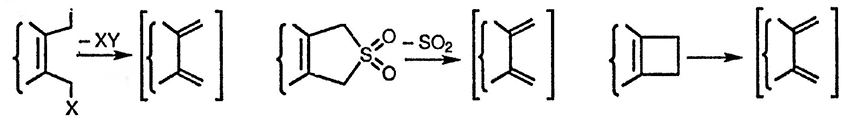
Основные стратегии, используемые для генерирования гетероциклических орто-хинодиметанов, связаны с реакцией 1,4-элиминирования, хелетропным элиминированием диоксида серы из 2,5-дигидротиофен-S,S-диоксидов и электроциклическим раскрытием цикла в циклобутеновых производных гетероциклических соединений. Каждый из этих процессов, приводящих к образованию орто-хинодиметанов, схематически приведён ниже:
Возможность использования циклобутеновых производных гетероциклических соединений безусловно определяется возможностью синтеза таких соединений (см., например, разд. 11.14.2.3.), однако в тех случаях, когда такие предшественники доступны, электроциклическое раскрытие циклобутенового цикла представляет собой наилучший способ генерирования орто-хинодиметанов. Раскрытие цикла происходит при простом нагревании циклобутеновых производных, как показано ниже. Первоначально образующийся аддукт Дильса—Альдера ароматизуется при взаимодействии с избытком хинона [18].
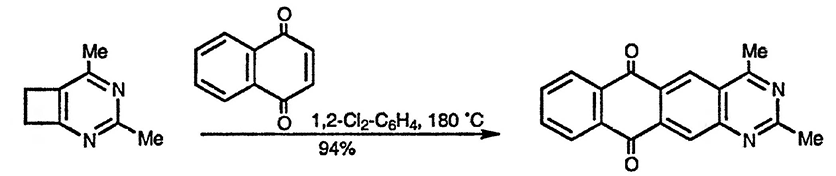
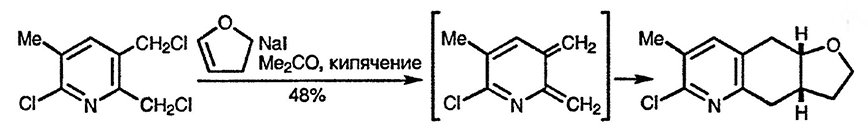
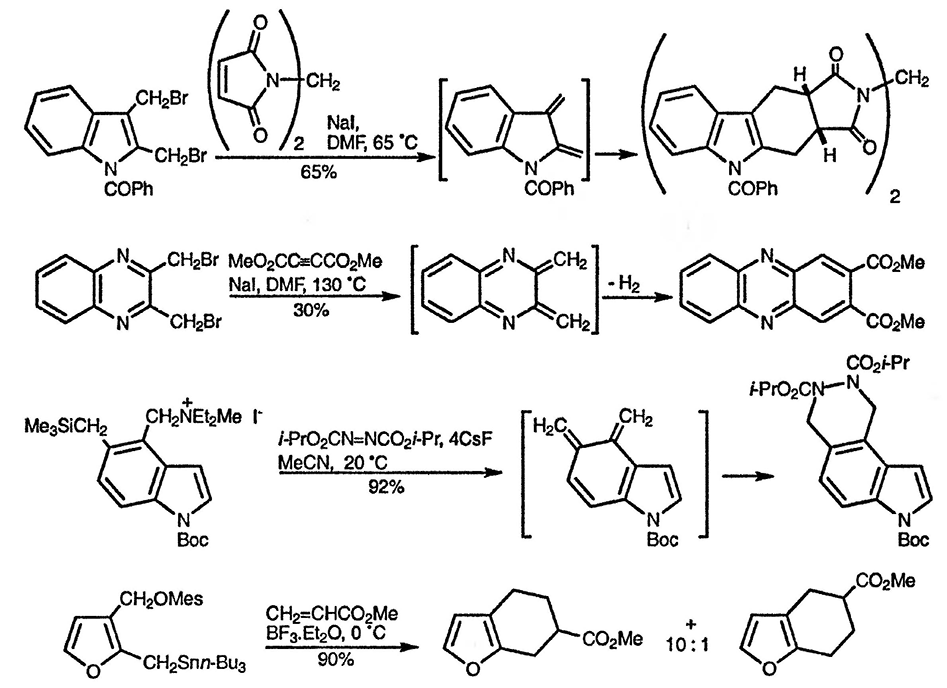
1,4-Элиминирование, приводящее к образованию орто-хинодиметана, может происходить при взаимодействии 1,2-бис(бромметил)производных гетероциклических соединений с йодидом натрия при нагревании [19], орто-(три-метилсилилметил)гетаренметиламмониевых солей [20] и мезитилатов орто-(триметилсилилметил)гетаренкарбинолов [21] с фторид-ионом или при реакции ацетатов орто-(три-н-бутилстаннилметил)гетаренкарбинолов с кислотами Льюиса [21].
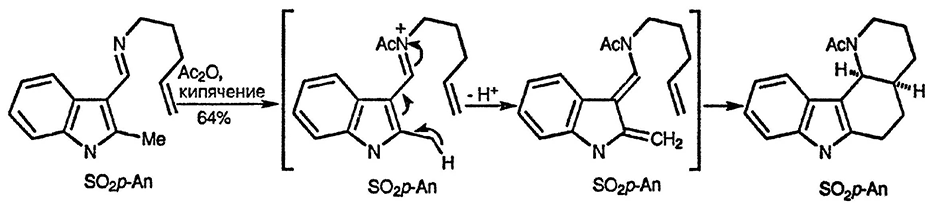
Метод, получивший в последние годы интенсивное развитие, — синтез индольных (и пиррольных [22]) орто-хинодиметанов путём депротонирования N-ацилированных иминов индол-3-илкарбальдегида, — показан на приведённой ниже схеме [23]:
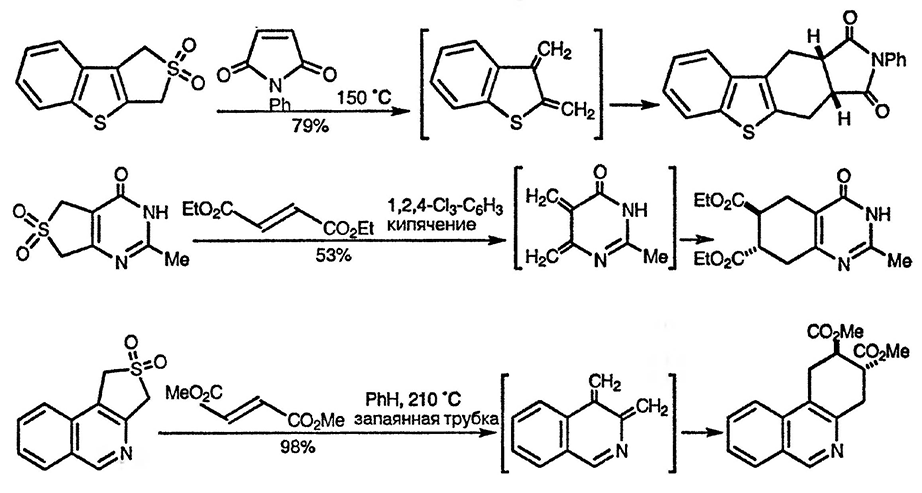
Наиболее общий метод генерирования орто-хинодиметанов, нашедший широкое применение, связан с экструзией молекулы диоксида серы из гетероциклических сульфонов. Сульфоны — предшественники орто-хинодиметанов — обычно стабильные соединения, легко получаются различными способами. Кроме того, кислотность протонов, соседних с сульфоновой группой, позволяет вводить заместители в такие молекулы при использовании оснований перед стадиями термической экструзии молекулы диоксида серы и реакции Дильса—Альдера. Ниже приведено несколько примеров генерирования орто-хинодиметанов таким способом [24]:
3.6. орто-Хинодиметаны в синтезе гетероциклических соединений
Список литературы к главе 3
Глава 3
- 3. Синтез ароматических гетероциклических соединений
- 3.1. Типы реакций, обычно используемые для синтеза гетероциклических соединений
- 3.2. Типичные комбинации реагентов
- 3.2.1.1 Синтез гетероароматических соединений
- 3.2.1.2. Синтез гетероароматических соединений
- 3.2.2. Вторая группа синтезов
- 3.3. Выводы
- 3.4. Электроциклические процессы в синтезе гетероциклических соединений
- 3.5. Нитрены в синтезе гетероциклических соединений
- 3.6. орто-Хинодиметаны в синтезе гетероциклических соединений
Дополнительно:
 Англо-русский словарь по химии и переработке нефти / English-Russian Dictionary of Petroleum Chemistry and Processing
Англо-русский словарь по химии и переработке нефти / English-Russian Dictionary of Petroleum Chemistry and Processing Словарь содержит около 60 000 терминов по нефтехимии и нефтепереработке, ...
Москва, 1958 год. Издательство Академии наук СССР. Издательский переплёт. ...
Книга представляет собой монографию по синтезу и свойствам стереоспецифических ...
