4.3. Общая характеристика
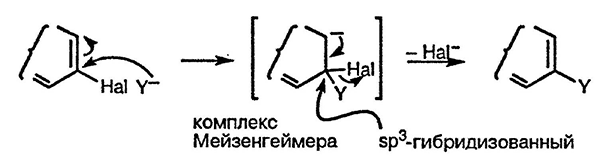
Нуклеофильное замещение в ароматических соединениях протекает как двухстадийный процесс: первоначально происходит присоединение нуклеофила (Y-), а затем элиминирование отрицательно заряженной частицы (чаще всего На1~), причём первая из этих стадий протекает медленнее и определяет скорость процесса в целом. Это так называемый механизм SNAE (Substitution Nucleophilic Addition Elimination — замещение нуклеофильное присоединение элиминирование).
Скорости замещения в различных положениях кольца можно оценить на основании рассмотрения структуры отрицательно заряженных интермедиатов (комплексов Мейзенгеймера), образующихся при присоединении нуклеофилов. При этом следует принимать во внимание, что относительная стабильность этих интермедиатов (степень делокализации отрицательного заряда) отражает относительную энергию переходных состояний, приводящих к этим интермедиатам. Например, 2- и 4-галогенонитробензолы вступают в реакции нуклеофильного замещения, поскольку образующиеся анионные аддукты стабилизированы в результате делокализации отрицательного заряда с участием нитрогруппы.
Электронодефицитный характер атомов углерода пиридинового цикла, особенно в положениях α и γ, приводит к тому, что реакции нуклеофильного присоединения и особенно реакции нуклеофильного замещения атома галогена (или другой хорошей уходящей группы), является важным аспектом химии пиридина.
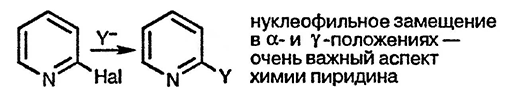
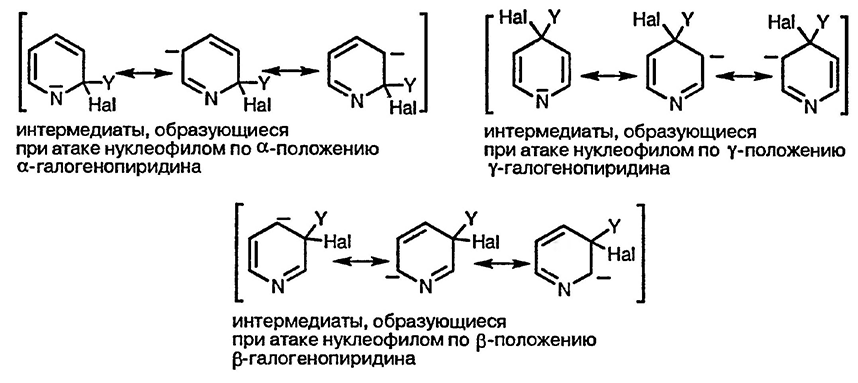
Нуклеофильное замещение в пиридинах протекает по тому же механизму, что и в случае 2- и 4-галогенонитробензолов, то есть первоначально происходит присоединение нуклеофила, а затем элиминирование галогенид-иона. Аналогично ситуации, характерной для производных бензола, присоединение нуклеофила облегчается пониженной электронной плотностью в α- и γ-положениях пиридина, что усиливается наличием галогенов в качестве заместителей в этих положениях и способностью гетероатома участвовать в делокализации отрицательного заряда. Сравнение трёх возможных интермедиатов наглядно демонстрирует, что участие гетероатома в делокализации отрицательного заряда невозможно при присоединении нуклеофила по β-положению. Таким образом, нуклеофильное замещение по β-положению характеризуется гораздо меньшей скоростью и для практических целей неприменимо.
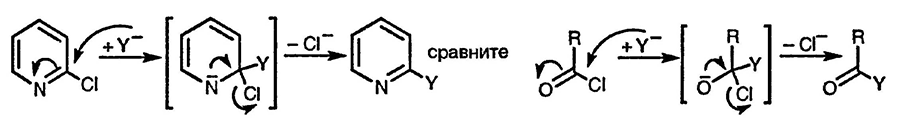
Полезно также сравнить реакционную способность α- и γ-галогенопиридинов с реакционной способностью ацилгалогенидов и β-галоген-α,β-непредельных кетонов. Для тех и других также характерно легко протекающее нуклеофильное замещение по механизму присоединение — элиминирование.
Метод введения заместителей (особенно углеродсодержащих) в ароматическое кольцо, использующий реакции предварительно генерированных металлированных производных ароматических соединений с электрофильными реагентами, приобретает все более важное значение. Атомы йода и брома в любом положении пиридинового кольца могут легко обмениваться с литием при низких температурах без побочных процессов нуклеофильного замещения или присоединения с образованием пиридиллитиевых производных.
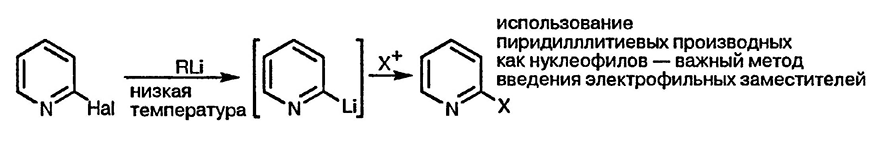
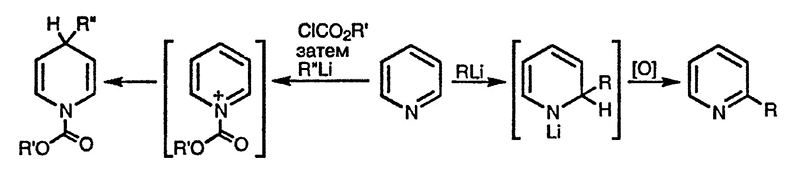
В отсутствие галогенных заместителей в α- и γ-положениях пиридиновый цикл менее активен в реакциях с нуклеофилами; кроме того, из-за отсутствия уходящей группы невозможно нуклеофильное замещение. Присоединение нуклеофилов, тем не менее, происходит, однако образующиеся при этом дигидропиридины требуют дальнейшего окисления для удаления «гидрид-иона» и завершения процесса замещения. Такие процессы, например с амидами металлов или металлоорганическими реагентами, протекают селективно по α-положению, вероятно, потому, что первоначально образуется комплекс, включающий взаимодействие кольцевого атома азота и катиона металла, связанного с реагентом. Наиболее ценный в синтетическом плане процесс связан с присоединением металлоорганических реагентов к N+-пиридиниевым солям. Образующиеся при этом дигидропиридины стабильны, поскольку атом азота включён в амидный или, чаще, уретановый фрагмент.
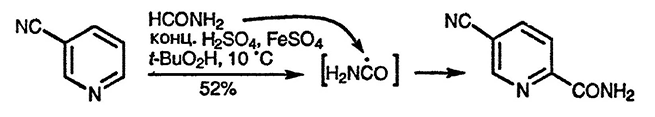
Реакции радикального замещения в пиридинах в кислых средах используются в настоящее время для препаративных целей. Для успешной реализации такого процесса радикальная частица должна обладать нуклеофильными свойствами, например *CH2OH, алкил- или ацил-радикалы. Пример реакции радикального аминокарбонилирования пиридина представлен ниже:
Пиридины с гидроксильными заместителями в α- и γ-положениях существуют в виде таутомеров с карбонильной группой — пиридонов. Тем не менее, наблюдается некоторое сходство реакционной способности пиридонов и фенолов. Так, пиридоны активированы к реакциям электрофильного замещения, причём замещение протекает по орто- и пара-положениям относительно кислородного заместителя. Пиридоны при потере атома водорода группы NH легко образуют анионы, которые по своей структуре и реакционной способности аналогичны фенолятам; в зависимости от условий возможны реакции таких анионов как по атому кислорода, так и по атому азота.
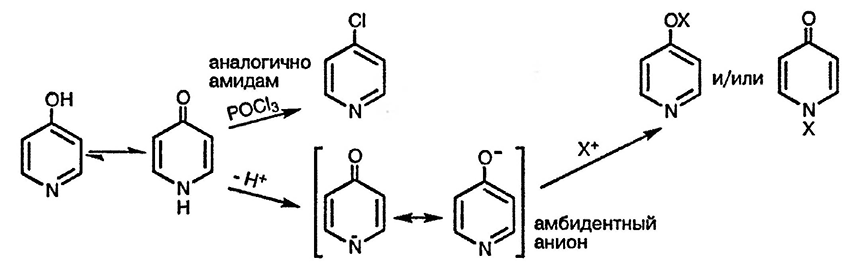
Основное отличие пиридонов от фенолов состоит в том, что первые способны под действием галогенидов фосфора и серы превращаться в соответствующие галогенопроизводные. В этом случае пиридоны реагируют аналогично амидам, и неорганические реагенты первоначально взаимодействуют с «амидным» атомом кислорода.
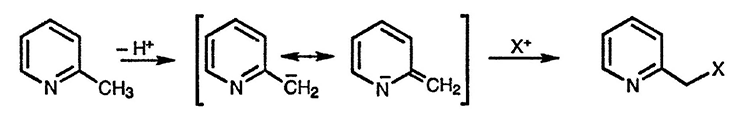
Пиридиновый цикл оказывает существенное влияние на алкильные заместители в α- и γ-положениях. Протоны алкильных групп в этих положениях обладают заметной подвижностью, поскольку образующийся при удалении этих протонов «енаминатный» анион стабилизирован в результате делокализации отрицательного заряда. Такое свойство алкильных групп в этих положениях чрезвычайно полезно для различных химических превращений в боковой цепи пиридина.
Пиридиниевые соли, как обсуждалось выше, весьма устойчивы к действию электрофильных агентов, но при этом легко вступают в реакции с нуклеофильными реагентами. Кислотность алкильных заместителей в α- и γ-положениях пиридиниевого катиона существенно выше, чем нейтрального алкилпиридина.
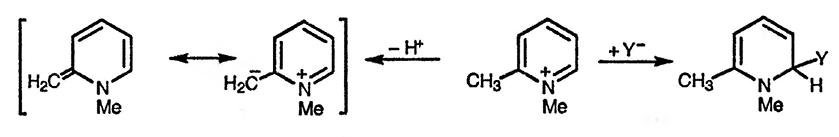
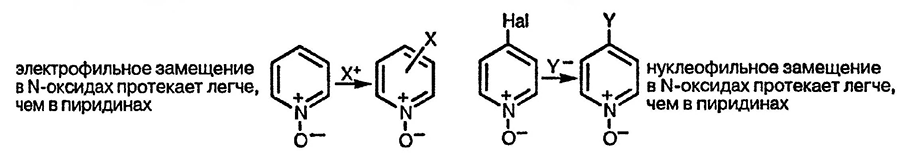
Пиридин-N-оксиды — особенно важные и полезные в синтетическом плане производные пиридина, не имеющие аналогий в ряду производных бензола. Строение N-оксидов пиридинов обеспечивает их большую склонность к реакциям электрофильного замещения и одновременно к реакциям с нуклеофилами по сравнению с самими пиридинами, что может показаться на первый взгляд удивительным. Действительно, с одной стороны, формально отрицательно заряженный атом кислорода пиридина-оксидов способен принимать участие в стабилизации интермедиатов реакции электрофильного замещения, а, с другой, положительно заряженный атом азота облегчает присоединение нуклеофилов.
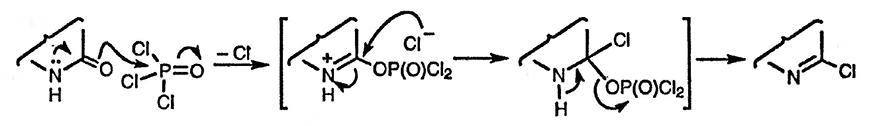
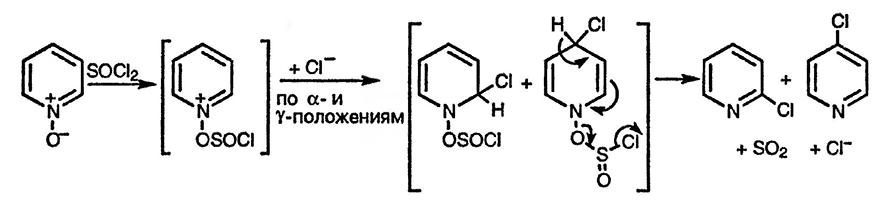
Существует ряд синтетически полезных процессов, в которых N-оксидная функция используется для введения заместителей в пиридиновый цикл (преимущественно в α-положение) и впоследствии удаляется. Реакция пиридин-N-оксида с тионилхлоридом представляет собой один из примеров таких процессов
Хинолин и изохинололин — две возможные структуры, в которых бензольное кольцо аннелировано к пиридиновому. Эти две структуры дают возможность обнаружить эффекты, возникающие при сочленении одного ароматического фрагмента с другим, то есть влияние бензольного кольца на реакционную способность пиридинового, и наоборот. Также следует рассмотреть свойства этих структур по сравнению со свойствами нафталина. Так, характерная для нафталина α-региоселектиность реакций электрофильного замещения наблюдается и в хинолине и в изохинолине — замещение проходит по положениям 5 и 8. Следует отметить, что электрофильное замещение в хинолине и изохинолине обычно включает атаку электрофильной частицей по аддукту гетероциклической молекулы с электрофилом (обычно протоном), что дезактивирует гетероцикл к реакциям с электрофилами.
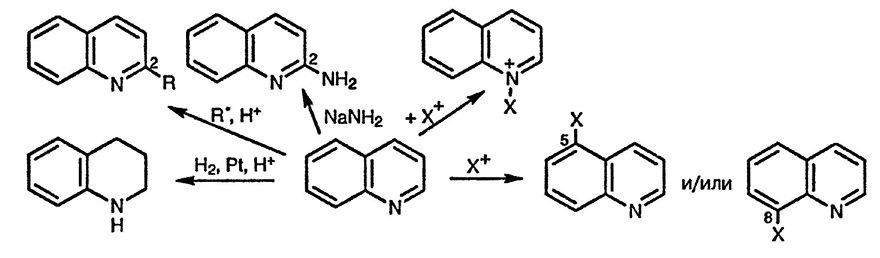
Точно также, как и в случае нафталина, предпочтительность атаки электрофилом по α-положению может быть объяснена при рассмотрении возможных интермедиатов; при электрофильной атаке по положениям 5/8 хинолина и изохинолина делокализация положительного заряда возможна без нарушения ароматичности пиридинового цикла. При атаке электрофилом по положениям 6/7 делокализация положительного заряда в образующихся интермедиатах возможна только с нарушением ароматичности пиридинового фрагмента.
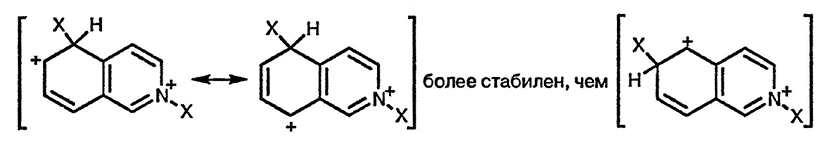
Таким образом, реакции хинолина и изохинолина с электрофильными реагентами протекают по бензольному кольцу, в то время как реакции с нуклеофильными реагентами — по пиридиновому. Особенно легко такие процессы проходят с участием α- и γ- положений (относительно атома азота) и, кроме того, эти положения в хинолине и изохинолине более чувствительны к атаке нуклеофилами, чем в самом пиридине. Последнее объясняется тем, что в образующихся интермедиатах полностью сохраняется ароматичность бензольного кольца. Поскольку энергия резонансной стабилизации бициклической ароматической структуры существенно меньше, чем двойная энергия стабилизации бензола или пиридина, то и потеря в энергии стабилизации при образовании промежуточных аддуктов из бициклических систем значительно ниже, чем в случае пиридина. Таким образом, рассматриваемая ситуация полностью аналогична ситуации, возникающей при сравнении реакционной способности бензола и нафталина по отношению к электрофильным агентам: скорость реакции электрофильного замещения в нафталине значительно выше, чем в бензоле, поскольку образование σ-комплексов из нафталина сопровождается меньшей потерей в энергии стабилизации.
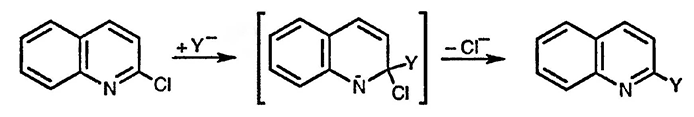
Существенные отличия от такого типичного поведения наблюдаются для положения 3 изохинолина — особая реакционная способность α-положения пиридина, которая обсуждалась выше, свойственна и для положения 1 изохинолина, но не для положения 3. Так, в случае нуклеофильного замещения в 3-гало-геноизохинолине в образующемся интермедиате невозможна делокализация отрицательного заряда без нарушения ароматичности бензольного кольца. В результате такой интермедиат значительно менее стабилен, и реакционная способность положения 3 изохинолина понижена.
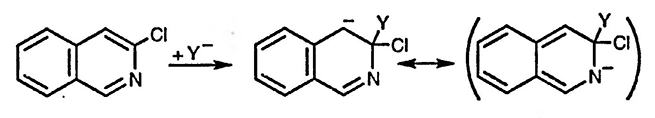
Атомы галогена во всех положениях пиридина и изохинолина можно заместить, используя каталитические реакции, обычно при применении палладия(0) в качестве катализатора (подробное обсуждение в см. разд. 2.7.). Реакции сочетания галогенопроизводных пиридинового ряда с алкенами (реакция Хека), алкинами, алкенильными и арильными соединениями олова и бора существенно дополняются реакциями сочетания металлоорганических (чаще оловоорганических) производных пиридина, хинолина и изохинолина с алкенил- или арилгалогенидами и трифлатами. Эта синтетическая методология чрезвычайно полезна и позволяет в одну стадию проводить такие превращения, успешное осуществление которых другими методами, если и возможно, то весьма затруднительно. Два примера использования этой методологии приведены ниже:
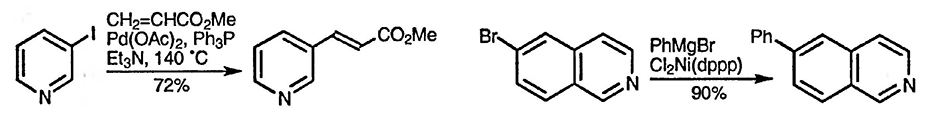
Существует огромное многообразие методов синтеза пиридинов. Наиболее очевидный подход к построению пиридинового цикла основан на реакции 1,5-дикарбонильных соединений, предпочтительно содержащих двойные связи, с аммиаком — присоединение аммиака по обеим карбонильным группам, сопровождающееся выделением воды, приводит к образованию пиридинового цикла. 1,4-Дигидропиридины, которые легко дегидрируются в полностью ароматические системы, можно получить при взаимодействии альдегида с двумя мольными эквивалентами 1,3-дикетона (или 1,3-кетоэфира) и аммиаком. Образование гетероцикла происходит в результате последовательно протекающих альдольной конденсации, реакции Михаэля и присоединении аммиака к концевым карбонильным группам на заключительной стадии.
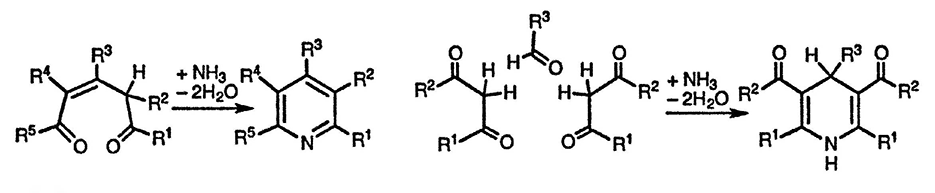
Практически все методы синтеза хинолинов используют в качестве исходных соединений ариламины. Как показано на приведённой ниже общей схеме, катализируемое кислотой взаимодействие ариламина с 1,3-дикарбо-нильным соединением включает присоединение аминогруппы к одной карбонильной группе и последующее замыкание ароматического цикла в результате реакции электрофильного замещения. Другой распространённый подход к синтезу хинолинов основан на реакции альдольного типа орто-аминобензальдегидов (или сходных по строению кетонов) с кетонами, обладающими α-метиленовой группой.
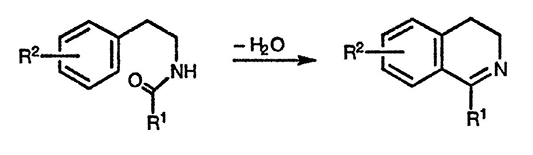
Замыкание цикла в амидах 2-арилэтиламинов приводит к образованию дигидроизохинолинов, которые легко дегидрируются в полностью ароматические соединения. Для такого замыкания цикла используется фосфорилхлорид в качестве реагента, а сам процесс циклизации представляет собой реакцию внутримолекулярного электрофильного замещения.
4.3. Общая характеристика
Глава 4
- 4. Общая характеристика реакционной способности пиридинов, хинолинов и изохинолинов
- 4.1. Электрофильное замещение при атоме углерода
- 4.2. Электрофильное замещение при атоме углерода
- 4.3. Общая характеристика
Дополнительно:
В монографии впервые в мировой литературе систематизирован и обобщён обширный ...
 Химические методы исследования синтетических смол и пластических масс
Химические методы исследования синтетических смол и пластических масс В книге описаны химические методы исследования синтетических смол и ...
В сборник включены наиболее интересные статьи по теории и практике переработки ...