27.1.1. Пирролидины и пиперидины
Эти азотсодержащие пяти- и шестичленные системы отличаются от своих ациклических аналогов главным образом тем, что они легко дегидрируются в соответствующие гетероароматические системы.
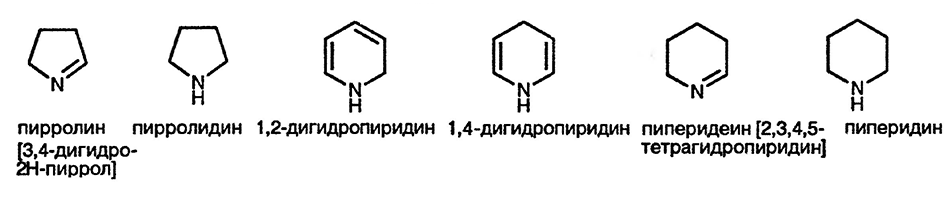
Вполне естественно, что способность ароматизоваться наиболее выражена для дигидроароматических систем; действительно, активность одного из важнейших восстановительных коферментов NADPH основана на такой тенденции, как показано ниже:
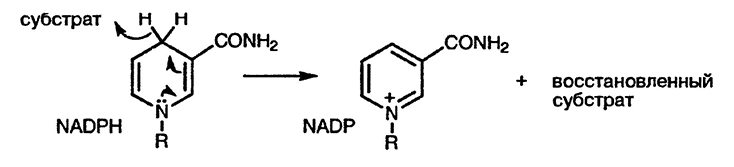
Дигидросоединения часто используются в качестве ценных синтетических интермедиатов; они обладают реакционной способностью, отличной от реакционной способности их гетероциклических аналогов. Например, индолины (2,3-дигидроиндолы) могут быть использованы для получения индолов [3], замещённых по бензольному кольцу, путём электрофильного замещения с последующей реароматизацией (разд. 17.16.1.); аналогично электрофильное замещение в дигидропиридинах, невозможное для самих пиридинов, даёт возможность при последующей реароматизации получать замещённые пиридины. Дегидрирование тетрагидро- и гексагидропроизводных требует гораздо более жёстких условий.
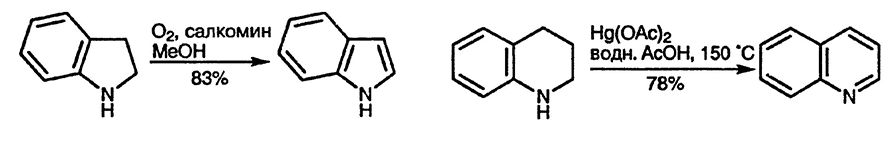
Вообще говоря, пиперидеины и пирролины существуют преимущественно в иминной форме, а не в таутомерной енаминной; N-алкилпроизводные не имеют альтернативы и существуют только в форме енаминов. Эти циклические имины устойчивы к гидролитическому расщеплению связи N=C в отличии от ациклических иминов, но тем не менее они легко вступают в реакции нуклеофильного присоединения по азометиновому атому углерода. Примером этому может служить тот факт, что и пиперидеин и пирролин существуют в виде тримеров, образующихся в результате нуклеофильного присоединения атома азота одной молекулы к азометиновому атому углерода другой молекулы, и так далее.
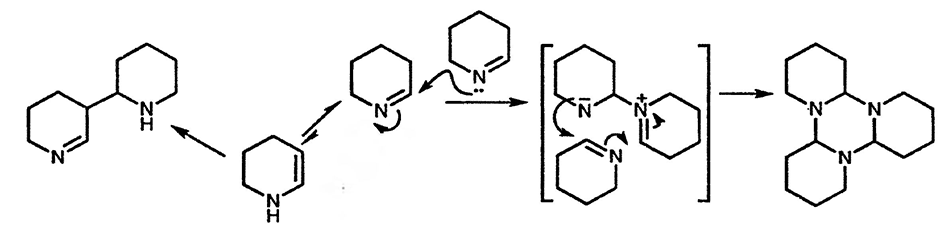
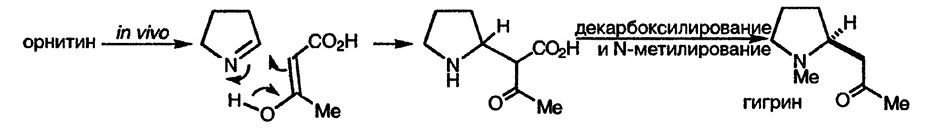
Присутствие в равновесии некоторого количества енамина проявляется при превращении пиперидеина в димер: действительно, способность этих двух систем выступать в роли как иминов, так и енаминов в конденсациях альдольного типа лежит в основе их участия в биосинтезе алкалоидов. Образующиеся в природе при окислительном дезаминировании и декарбоксилировании орнитина и лизина, они становятся фрагментами алкалоидных структур при конденсации с фрагментами других предшественников [4]. В качестве простого примера можно привести гигрин, в котором 1-пирролин в иминной форме конденсируется с ацетоацетатом или его эквивалентом.
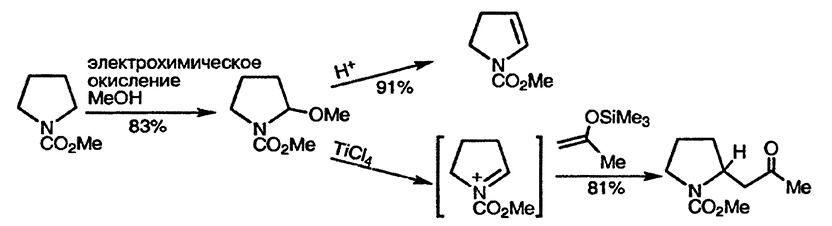
Контролируемое окисление N-ацилпиперидинов и N-ацилпирролидинов может быть использовано для получения 2-алкоксипроизводных или эквивалентных им енамидов, которые представляют собой полезные синтетические интермедиаты [5]. Первые легко вступают в реакции нуклеофильного замещения в условиях катализа кислотами Льюиса, образуя интермедиаты типа Манниха, а вторые могут подвергаться электрофильному замещению по атому C(3) или присоединению по двойной связи.
Пирролидин и пиперидин — более активные нуклеофилы, чем диэтиламин, главным образом за счёт того, что свободные пары электронов атома азота менее заслонены — в гетероциклах два «алкильных» заместителя при атоме азота, то есть кольцевые атомы углерода, зафиксированы и в меньшей степени экранируют свободные электронные пары. Таким образом, приближающийся электрофил не встречает тех препятствий, которые возникают в диэтиламине из-за вращения вокруг связей C—N и C–C. Значения pKa пирролидина (11,27) и пиперидина (11,29) характеризуют их как типичные аминные основания, и их основность немного превышает основность диэтиламина (10,98).
Пиперидины, подобно циклогексану, принимают конформацию кресла. Направление ориентации свободной пары и ориентации связанных с атомом азота заместителей (или атома водорода) в пиперидинах стало предметом многих дискуссий; некоторая путаница возникает при проведении реакций N-алкилирования, образующиеся при этом соединения не всегда отражают заселённость основной конформации. И атом водорода, и алкильная группа при атоме азота принимают экваториальную ориентацию, хотя в последнем случае преобладание экваториального изомера незначительно [6].
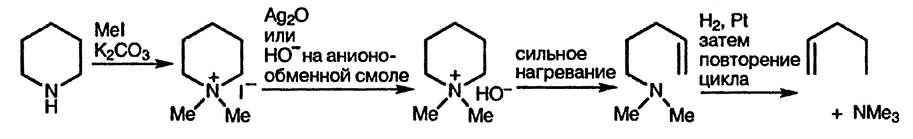
Раньше строение природных соединений определяли методом их деградации. Многие алкалоиды содержат в своём составе насыщенные азотистые гетероцилы, поэтому метод деградации позволяет определить окружение атома азота, обладающего основными свойствами. В качестве классического использовался метод исчерпывающего алкилирования по Гофману. Этот метод приводит к расщеплению связей C—N гетероцикла и, в конечном итоге, к удалению атома азота; повторение процедуры требуется для удаления атома азота, первоначально входящего в цикл, а проведение третьего цикла превращений необходимо в том случае, когда два кольца содержат общий атом азота. На основании данных о строении безазотистых фрагментов устанавливают структуру исходного углеродного скелета.
27.1.1. Пирролидины и пиперидины
Список литературы к главе 27
Глава 27
- 27. Насыщенные и частично ненасыщенные гетероциклические соединения: реакции и методы синтеза
- 27.1. Пяти- и шестичленные циклы
- 27.1.1. Пирролидины и пиперидины
- 27.1.2. Пираны и восстановленные фураны
- 27.2. Трёхчленные циклы
- 27.2.1. Трёхчленные циклы с одним гетероатомом
- 27.2.2. Трёхчленные гетероциклы с двумя гетероатомами
- 27.3. Четырёхчленные циклы
- 27.4. Металлирование
- 27.5. Синтезы кольца
- 27.5.1. Насыщенные азотсодержащие гетероциклы
- 27.5.2. Насыщенные кислородсодержащие гетероциклы
- 27.5.3. Насыщенные серосодержащие гетероциклы
Дополнительно:
В книге рассмотрен весь комплекс оборудования, применяемого не только для ...
 Теория периодической системы
Теория периодической системы В учебном пособии изложена обобщённая теория периодической системы как ...
 Новые методы препаративной органической химии
Новые методы препаративной органической химии Москва, 1950 год. Издательство иностранной литературы. Издательский переплёт. ...
 Цианистые соединения и их анализ
Цианистые соединения и их анализ Воспроизведено в оригинальной авторской орфографии издания 1933 года ...