2.1. Реакции электрофильного присоединения к атому азота
В гетероциклических соединениях, содержащих иминовый фрагмент (C=N) как составную часть структуры — пиридинах, хинолинах, изохинолинах, 1,2- и 1,3-азолах и других, неподелённая электронная пара атома азота не включена в ароматическую π-систему (разд. 1.2.) и, следовательно, способна к взаимодействию с электрофильными реагентами аналогично простым аминам. Другими словами, такие гетероциклические соединения проявляют свойства оснований и способны присоединять протон и другие электрофилы по атому азота. Образующиеся при этом соли могут быть выделены.
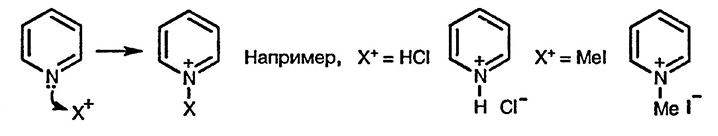
В случае обратимых реакций присоединения, например, протонирования, положение равновесия определяется значением pKa гетероциклического соединения [1] и зависит от заместителей, присутствующих в гетероцикле. Электронодонорные заместители увеличивают основность, а электроноакцепторные понижают силу основания. Значения pKa простых производных пиридина близко к 5, основность 1,2- и 1,3-азолов зависит от характера второго гетероатома, а для пиразола и имидазола, содержащих два атома азота, значение pKa равно соответственно 2,5 и 7,1.
Нуклеофильность атома азота иминного фрагмента коррелирует с основностью, хотя и не всегда. Заместители у атома углерода, соседнего с иминым атомом азота, могут оказывать существенное влияние на лёгкость протекания реакции с алкилгалогенидами, приводящей либо к образованию соответствующих N+-алкильных солей [2], либо N+H-солей в результате 1,2-элиминирования молекулы галогеноводорода. Показано, что скорость реакции N-алкилирования уменьшается в 3 раза за счёт стерического взаимодействия при введении одной метальной группы в α-положение к атому азота пиридина, а введение двух метальных групп в положения 2 и 6 уменьшает скорость реакций алкилирования в 12-40 раз [3].
Экстремальный случай — 2,6-ди-трет-бутилпиридин, который не алкилируется метилиодидом даже при повышенном давлении; метилирование такого производного пиридина может быть осуществлено при использовании чрезвычайно реакционноспособного метилового эфира фторсульфоновой кислоты при высоком давлении [4]. Количественная оценка реакционной способности атома азота определяется как стерическими (особенно при наличии заместителя в α-положении), так и электронными эффектами: так, 3-метилпи-ридин реагирует быстрее (х 1,6) незамещённого пиридина, а 3-хлорпиридин — медленнее (х 0,14). Заместители в пери-положении оказывают существенное влияние на скорость реакции с метилодидом: так, скорости реакции пиридина, изохинолина (отсутствует атом водорода в пери-положении), хинолина и 8-метилхинолина равны соответственно 50,69,8 и 0,008.
На скорость образования четвертичных солей оказывают влияние также и другие факторы. Например, все диазины взаимодействуют с метилиодидом медленнее, чем пиридин. Пиридазин, хотя и представляет собой наиболее слабое среди диазинов основание по сравнению с пиридином (pKa 2,3), реагирует с метилиодидом быстрее, чем другие диазины. Связано это с проявлением «α-эффекта», то есть увеличением нуклеофильности в результате взаимного отталкивания неподелённых пар электронов двух непосредственно связанных атомов азота [5]. Скорости реакций с метилиодидом пиридазина, пиримидина и пиразина относительно пиридина составляют 0,25,0,044 и 0,036 соответственно.
2.1. Реакции электрофильного присоединения к атому азота
Список литературы к главе 2
Глава 2
- 2. Реакционная способность ароматических гетероциклических соединений
- 2.1. Реакции электрофильного присоединения к атому азота
- 2.2. Реакции электрофильного замещения при атому углерода
- 2.2.1. Механизм ароматического электрофильного замещения
- 2.2.2. Шестичленные гетероциклические соединения
- 2.2.3. Пятичленные гетероциклические соединения
- 2.3. Реакции нуклеофильного замещения при атоме углерода
- 2.3.1. Механизм реакции ароматического нуклеофильного замещения
- 2.3.2. Шестичленные гетероциклические соединения
- 2.3.3. Викариозное нуклеофильное замещение
- 2.4. Реакции радикального замещения при атоме углерода
- 2.4.1. Реакции гетероциклических соединений с нуклеофильными радикалами. Реакция Минисци
- 2.4.2. Реакции с электрофильными радикалами
- 2.5. Депротонирование атома азота
- 2.6. Металлоорганические производные
- 2.6.1. Литийорганические производные
- 2.6.1.1. Прямое литиирование (депротонирование при атоме углерода)
- 2.6.1.2. Обмен атома галогена
- 2.6.1.3. Литиирование пятичленных гетероциклических соединений
- 2.6.1.4. Литиирование шестичленных гетероциклических соединений
- 2.6.2. Магнийорганические производные
- 2.6.3. Бор-, кремний- и оловоорганические реагенты
- 2.6.3.1. Синтез
- 2.6.3.2. Реакции
- 2.6.4. Цинкорганические производные
- 2.6.5. Металлирование боковой цепи шестичленных гетероциклических соединений («латеральное металлирование»)
- 2.6.6. Металлирование боковой цепи пятичленных гетероциклических соединений
- 2.7. Реакции, катализируемые палладием
- 2.7.1. Основные процессы с участием палладийорганических соединений
- 2.7.1.1. Согласованные реакции
- 2.7.1.2. Ионные реакции
- 2.7.2. Реакции, катализируемые палладием, в химии гетероциклических соединений
- 2.7.2.1. Реакция Хека
- 2.7.2.2. Реакции сочетания
- 2.7.2.3. Реакции карбонилирования
- 2.7.2.4. Синтез бензоконденсированных гетероциклических соединений
- 2.8. Окисление и восстановление гетероциклических соединений
- 2.9. Биологические процессы в химии гетероциклических соединений
Дополнительно:
 Технология переработки кристаллических полиолефинов
Технология переработки кристаллических полиолефинов Монография обобщает сведения о технологии основных процессов переработки ...
Сборник содержит статьи, посвящённые применению колебательных спектров для ...
 Популярная библиотека химических элементов (комплект из 2 книг)
Популярная библиотека химических элементов (комплект из 2 книг) Популярная библиотека химических элементов" составлена из рассказов и заметок ...
Содержатся данные о физических и термодинамических свойствах свыше 1 800 веществ, а ...