2.3.3. Викариозное нуклеофильное замещение
Процессы, известные как реакции «викариозного нуклеофильного замещения» атома водорода (в англоязычной литературе принято обозначение VNS — Vicarious Nucleophilic Substitution), широко применимы как к карбоциклическим, так и гетероциклическим ароматическим соединениям [41].
Обычно для реализации такого нуклеофильного замещения необходимо присутствие нитрогруппы в молекуле субстрата, что обеспечивает возможность присоединения углеродного нуклеофила, образующегося из C(X)(Y)(R), где X — потенциально уходящая группа, a Y — группа, стабилизирующая анион. Присутствие электроноакцепторной группы Y позволяет также получить в результате депротонирования соответствующий анион на первой стадии процесса. Наиболее часто X представляет собой атом галогена, a Y — арилсульфонильную группу. Типичная последовательность превращений при викариозном нуклеофильном замещении приведена ниже.
Первоначально происходит присоединение углеродного нуклеофила по орто- или пара-положению относительно нитрогруппы, затем элиминирование молекулы НХ из образующегося в результате присоединения сопряжённого неароматического нитроната, а затем последующее протонирование приводит к образованию ароматической молекулы продукта замещения. Обычно в таких процессах используется избыток основания, который генерирует карбанион и направляет процесс дальше за счёт отщепления и необратимого связывания молекулы НХ.
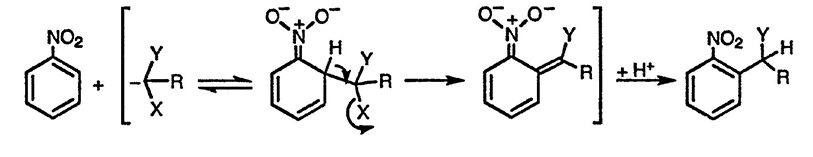
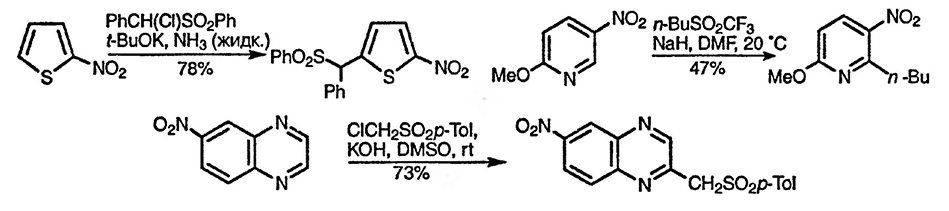
Примеры реакций викариозного нуклеофильного замещения даны в некоторых последующих главах книги. Ниже приведены три типичных примера таких превращений. Первый пример связан с реакцией викариозного нуклеофильного замещения в пятичленных гетероциклических соединениях [42]. Во втором примере стабилизирующая анион трифторметансульфонильная группа (Y) одновременно служит и уходящей группой (X) [43]. Третий пример в некоторой степени необычен, поскольку нуклеофил присоединяется не по орта- или пара-положению относительно нитрогруппы. Присоединение карбаниона проходит по положению C(2) 6-нитрохиноксалина; образующийся в результате такого присоединения анион стабилизирован делокализацией отрицательного заряда одновременно с участием атома азота N(1) и нитрогруппы [44].
2.3.3. Викариозное нуклеофильное замещение
Список литературы к главе 2
Глава 2
- 2. Реакционная способность ароматических гетероциклических соединений
- 2.1. Реакции электрофильного присоединения к атому азота
- 2.2. Реакции электрофильного замещения при атому углерода
- 2.2.1. Механизм ароматического электрофильного замещения
- 2.2.2. Шестичленные гетероциклические соединения
- 2.2.3. Пятичленные гетероциклические соединения
- 2.3. Реакции нуклеофильного замещения при атоме углерода
- 2.3.1. Механизм реакции ароматического нуклеофильного замещения
- 2.3.2. Шестичленные гетероциклические соединения
- 2.3.3. Викариозное нуклеофильное замещение
- 2.4. Реакции радикального замещения при атоме углерода
- 2.4.1. Реакции гетероциклических соединений с нуклеофильными радикалами. Реакция Минисци
- 2.4.2. Реакции с электрофильными радикалами
- 2.5. Депротонирование атома азота
- 2.6. Металлоорганические производные
- 2.6.1. Литийорганические производные
- 2.6.1.1. Прямое литиирование (депротонирование при атоме углерода)
- 2.6.1.2. Обмен атома галогена
- 2.6.1.3. Литиирование пятичленных гетероциклических соединений
- 2.6.1.4. Литиирование шестичленных гетероциклических соединений
- 2.6.2. Магнийорганические производные
- 2.6.3. Бор-, кремний- и оловоорганические реагенты
- 2.6.3.1. Синтез
- 2.6.3.2. Реакции
- 2.6.4. Цинкорганические производные
- 2.6.5. Металлирование боковой цепи шестичленных гетероциклических соединений («латеральное металлирование»)
- 2.6.6. Металлирование боковой цепи пятичленных гетероциклических соединений
- 2.7. Реакции, катализируемые палладием
- 2.7.1. Основные процессы с участием палладийорганических соединений
- 2.7.1.1. Согласованные реакции
- 2.7.1.2. Ионные реакции
- 2.7.2. Реакции, катализируемые палладием, в химии гетероциклических соединений
- 2.7.2.1. Реакция Хека
- 2.7.2.2. Реакции сочетания
- 2.7.2.3. Реакции карбонилирования
- 2.7.2.4. Синтез бензоконденсированных гетероциклических соединений
- 2.8. Окисление и восстановление гетероциклических соединений
- 2.9. Биологические процессы в химии гетероциклических соединений
Дополнительно:
В книге изложены современные теоретические представления об основных процессах ...
Москва, 1958 год. Издательство Академии наук СССР. Издательский переплёт. ...
Дипольный момент — важная молекулярная константа, характеризующая ...
Настоящая монография ставит своей задачей дать по возможности полное обобщение ...