2.6.1.1. Прямое литиирование (депротонирование при атоме углерода)
Большинство гетероциклических соединений при взаимодействии с алкиллитиевыми соединениями или амидами лития превращается в результате отщепления протона в соответствующие литиевые производные. Хотя и «свободные» анионы никогда при этом не образуются, лёгкость литиирования связана с кислотностью атома водорода при атоме углерода и, соответственно, со стабильностью сопряжённого основания (карбаниона) [61].
Прямое литиирование в результате депротонирования напрямую связано с катализируемым основанием протонным обменом [62] при использовании таких реагентов, как метилат натрия. Именно такие процессы, проводимые при температурах, значительно более высоких, чем требуется для прямого литиирования, впервые продемонстрировали возможность селективного проведения процессов депротонирования и их использования в синтетических целях. Следует помнить, что кинетические факторы и положение кислотного равновесия не всегда способствуют одному и тому же направлению процесса: термодинамически более стабильные продукты депротонирования обычно образуются при повышенной температуре и при проведении реакции в более полярных растворителях.
Детали механизма прямого металлирования всё ещё остаётся предметом дискуссий, возможно процесс включает четырёхцентровое переходное состояние
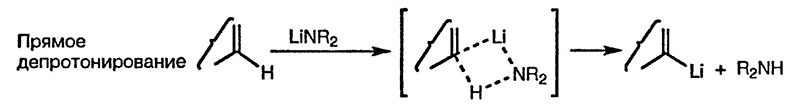
Основной фактор, приводящий к увеличению кислотности атома водорода, связанного с атомом углерода гетероцикла — индуктивный эффект гетероатома или гетероатомов. Вследствие этого прямое литиирование проходит по α-положению относительно гетероатома, поскольку в этом положении индуктивный эффект проявляется наиболее сильно. Однако такое направление процесса прямого литиирования может быть изменено под влиянием других факторов, которые обсуждаются ниже.
Мезомерия
«Анионная» орбиталь во всех случаях, за исключением тех, в которых анионный центр расположен в боковой цепи гетероциклического соединения, ортогональна π-системе и по этой причине не взаимодействует с ней мезомерно. Тем не менее, на электронную плотность и, следовательно, на кислотность атомов водорода, связанных с атомами углерода гетероцикла, оказывает влияние резонансный эффект.
Координация металла с гетероатомом
Сильная координация между металлом основания и гетероатомом приводит к увеличению СН-кислотности вследствие индуктивного оттягивания электронной плотности, которое проявляется в большей степени в случае кислорода, чем в случае серы.
Взаимодействия неподелённой пары электронов
Взаимное отталкивание между «анионной» орбиталью и неподелённой парой электронов гетероатома оказывает дестабилизирующее влияние на анион. Этот эффект особенно проявляется в производных пиридина и диазинов [63].
Поляризуемость гетероатома
Гетероатомы, способные к поляризации, такие, как сера, способствуют эффективному «рассеиванию» отрицательного заряда.
Эффекты заместителя
Процессы направленного металлирования имеют очень важное значение в химии гетероциклических соединений. Металлирование в орто-положение относительно ориентирующей группы может быть обусловлено либо индуктивным эффектом (такие группы, как Cl, F), либо эффектом хелатирования (CH2OH → CH2OLi), либо совокупностью обоих эффектов. Причём в некоторых случаях эффекты направляющих групп могут изменять «обычную» региоселективность при металлировании гетероциклических соединений. В том случае, когда проявление такого эффекта возможно, он оказывает наиболее сильное влияние на региоселективность процесса металлирования.
Литиирующие агенты
Обычно прямое литиировании проводят с использованием алкиллитиевых соединений или амидов лития. Наиболее широко используется и-бутиллитий, однако в том случае, когда необходимо использовать более эффективный литиирующий агент, применяют втор-бутиллитий, а иногда и трет-бутиллитий. Ранее широкое применение находил фениллитий; в последнее время этот реагент практически не используется, однако в тех случаях, когда необходим менее активный и более селективный литиирующий агент, фениллитий может оказаться весьма полезным [65]. Наиболее сильный металлирующий агент получают из смеси н-бутиллития и трет-бутилата калия; при использовании этого металлирующего агента получаются калиевые производные гетероциклических соединений.
Среди амидов лития наиболее часто используемый литиирующий агент — диизопропиламид лития (LDA). 2,2,6,6-Тетраметилпиперидит лития (LiTMP) — более основный и менее нуклеофильный агент — нашел широкое применение при литиировании диазинов. Алкиллитиевые соединение — основания более сильные, чем амиды лития, хотя обычно литиирование с использованием алкил" литиевых реагентов проходит медленно. Металлирование амидами лития обратимо и, следовательно, эффективное превращение гетероциклических субстратов возможно в том случае, если их кислотность (рКа > 4) выше, чем кислотность соответствующих амидов.
Растворители
Обычно для проведения таких реакций используют эфирные растворители — диэтиловый эфир и тетрагидрофуран. Более сильные координирующие свойства, присущие тетрагидрофурану, повышают активность литиирующих агентов, так как увеличивают степень их диссоциации. Смесь эфира, ТГФ и пентана используется для проведения реакций при очень низких температурах (—100 °C, чистый ТГФ замерзает при этих температурах). Для увеличения активности литиирующих агентов в реакционную смесь в некоторых случаях добавляют лиганды, способные к сильной координации по катиону металла, такие, как N,N,N,N-тетраметилэтилендиамин (TMEDA) или гексаметилтриамид фосфорной кислоты (канцероген). Несмотря на то, что применение таких добавок в ряде случаев несомненно приводит к успешному металлированию, эффективность TMEDA служит предметом обсуждений [66].
2.6.1.1. Прямое литиирование (депротонирование при атоме углерода)
Список литературы к главе 2
Глава 2
- 2. Реакционная способность ароматических гетероциклических соединений
- 2.1. Реакции электрофильного присоединения к атому азота
- 2.2. Реакции электрофильного замещения при атому углерода
- 2.2.1. Механизм ароматического электрофильного замещения
- 2.2.2. Шестичленные гетероциклические соединения
- 2.2.3. Пятичленные гетероциклические соединения
- 2.3. Реакции нуклеофильного замещения при атоме углерода
- 2.3.1. Механизм реакции ароматического нуклеофильного замещения
- 2.3.2. Шестичленные гетероциклические соединения
- 2.3.3. Викариозное нуклеофильное замещение
- 2.4. Реакции радикального замещения при атоме углерода
- 2.4.1. Реакции гетероциклических соединений с нуклеофильными радикалами. Реакция Минисци
- 2.4.2. Реакции с электрофильными радикалами
- 2.5. Депротонирование атома азота
- 2.6. Металлоорганические производные
- 2.6.1. Литийорганические производные
- 2.6.1.1. Прямое литиирование (депротонирование при атоме углерода)
- 2.6.1.2. Обмен атома галогена
- 2.6.1.3. Литиирование пятичленных гетероциклических соединений
- 2.6.1.4. Литиирование шестичленных гетероциклических соединений
- 2.6.2. Магнийорганические производные
- 2.6.3. Бор-, кремний- и оловоорганические реагенты
- 2.6.3.1. Синтез
- 2.6.3.2. Реакции
- 2.6.4. Цинкорганические производные
- 2.6.5. Металлирование боковой цепи шестичленных гетероциклических соединений («латеральное металлирование»)
- 2.6.6. Металлирование боковой цепи пятичленных гетероциклических соединений
- 2.7. Реакции, катализируемые палладием
- 2.7.1. Основные процессы с участием палладийорганических соединений
- 2.7.1.1. Согласованные реакции
- 2.7.1.2. Ионные реакции
- 2.7.2. Реакции, катализируемые палладием, в химии гетероциклических соединений
- 2.7.2.1. Реакция Хека
- 2.7.2.2. Реакции сочетания
- 2.7.2.3. Реакции карбонилирования
- 2.7.2.4. Синтез бензоконденсированных гетероциклических соединений
- 2.8. Окисление и восстановление гетероциклических соединений
- 2.9. Биологические процессы в химии гетероциклических соединений
Дополнительно:
 Естествознание и проблема белка. Химическое и пространственное строение белков. Структурная организация белков
Естествознание и проблема белка. Химическое и пространственное строение белков. Структурная организация белков В книге прослежены этапы развития исследований химического и пространственного ...
 Физика нефтяного и газового пласта
Физика нефтяного и газового пласта Рассмотрены физико-химические свойства пластовых жидкостей и газов, ...
 Комплексы 4d-платиновых металлов с фосфор(III)- и мышьяк(III)- органическими лигандами
Комплексы 4d-платиновых металлов с фосфор(III)- и мышьяк(III)- органическими лигандами В монографии проанализированы и обобщены данные по условиям стабилизации ...