22.12. Окси- и амино-1,2-азолы
Только 4-гидрокси-1,2-азолы можно рассматривать как соединения, подобные фенолу [76]. 3- и 5-Гидрокси-1,2-азолы существуют преимущественно в карбонильных таутомерных формах, что обусловлено участием гетероатома в стабилизации резонансных структур; таким образом, эти соединения известны как пиразолоны, изоксазолоны и изотиазолоны, хотя для всех трёх систем в зависимости от природы других заместителей в растворе наблюдается присутствие заметного количества гидроксиизомеров.
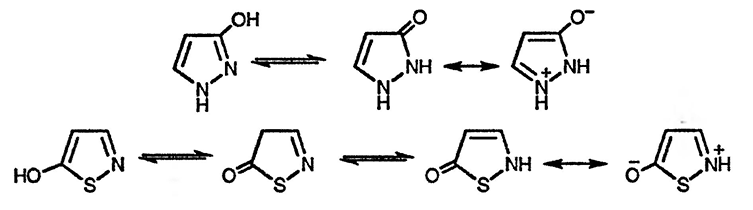
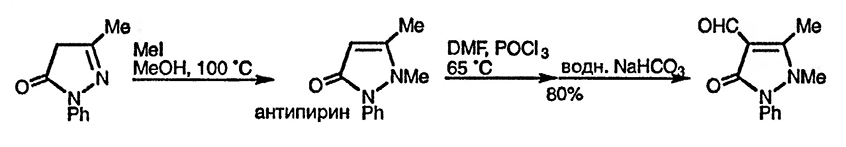
При изучении и использовании реакций 3- и 5-азолонов основное внимание уделяется их способности реагировать с электрофилами, такими, как галогены [77] (при этом образуются 4,4-дигалогенопроизводные с избытком реагента, например 4,4-дибром-3-метилпиразол-5-он — пара-селективный бромирующий агент для фенолов и анилинов [78]) или нитраты [79], а также вступать в реакцию формилирования по Вильсмейеру [80]. На приведённом ниже примере показано формилирование антипирина, используемого в качестве анальгетика. Многие красители получают на основе реакции сочетания катионов арилдиазония с 5-пиразолонами по положению 4, один из таких примеров — тартазин.
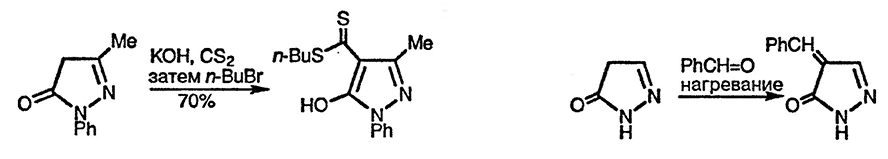
Пиразолоны также конденсируются с альдегидами [81] по альдольному типу или реагируют с другими электрофилами, например с сероуглеродом [82], и в обоих случаях в реакции предположительно участвует енольный таутомер или его анион. В основных растворах 3-изоксазолоны алкилируются либо по атому азота, либо по атому кислорода, и выбор основания может влиять на направление реакции [42].
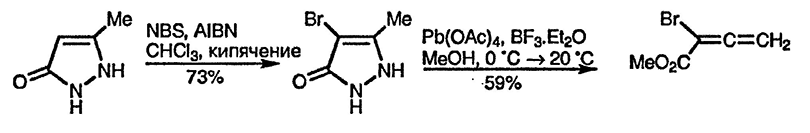
Интригующий и одновременно простой синтез полезного бромаллена основан на окислении бромпиразола ацетатом свинца(ГУ) [83]
Амино-1,2-азолы существуют в аминной таутомерной форме. Аминопиразолы и аминоизотиазолы ведут себя подобно ароматическим аминам: так, например, 3(5)-аминопиразол ацетилируется по аминогруппе и легко электрофильно бромируется по положению 4 [84]. Диазотирование и последующая реакция Зандмейера позволяют получать галогенизотиазолы [52] и азидопиразолы [85].

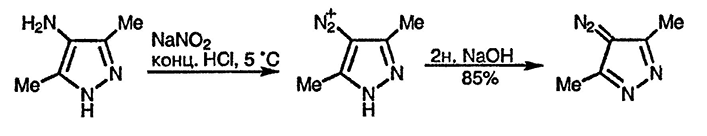
Диазотированием 4-аминопиразолов с последующим депротонированием получают устойчивые диазопиразолы [86].
Глава 22
- 22. 1,2-азолы-пиразолы, изотиазолы и изоксазолы: реакции и методы синтеза
- 22.1. Реакции с электрофильными реагентами
- 22.1.1. Присоединение по атому азота
- 22.1.1.1. Протонирование
- 22.1.1.1. Окисление по атому азота
- 22.1.1.3. Алкилирование по атому азота
- 22.1.1.4. Ацилирование по атому азота
- 22.1.2. Реакции замещения по атому углерода
- 22.1.2.1. Нитрование
- 22.1.2.2. Сульфирование
- 22.1.2.3. Галогенирование
- 22.1.2.4. Ацилирование
- 22.2. Реакции с окислителями
- 22.3. Реакции с нуклеофильными реагентами
- 22.4. Реакции с основаниями
- 22.4.1. Депротонирование группы NH пиразола
- 22.4.2. Депротонирование СН
- 22.5. Реакции N-металлированных пиразолов
- 22.6. Реакции C-металлированных 1,2-азолов
- 22.7. Реакции со свободными радикалами
- 22.8. Реакции с восстановителями
- 22.9. Электроциклические реакции
- 22.10. Алкилпроизводные 1,2-азолов
- 22.11. Четвертичные соли 1,2-азолов
- 22.12. Окси- и амино-1,2-азолы
- 22.13. Синтезы 1,2-азолов
- 22.13.1. Синтезы кольца
- 22.13.1.1. Из 1,3-дикарбонильных соединений и гидразинов или гидроксиламина
- 22.13.1.2. Диполярное циклоприсоединение нитрилоксидов и нитрилиминов
- 22.13.1.3. Из оксимов и гидразонов
- 22.13.2. Примеры некоторых важных синтезов с использованием 1,2-азолов
- 22.13.2.1. 5-Циан-1,2,6,7,12,12b-гексагидроиндоло[2,3-a]хинолизин
- 22.13.2.2. 3-Ацетилиндол
Дополнительно:
 Применение полимерных материалов в качестве покрытий
Применение полимерных материалов в качестве покрытий Широкое развитие производства полимерных материалов, постоянное улучшение их ...
 Методы и достижения в физико-органической химии
Методы и достижения в физико-органической химии Сборник содержит фундаментальные обзоры из двух широко известных зарубежных ...
 Коррозия и способы защиты оборудования в сернокислотной промышленности
Коррозия и способы защиты оборудования в сернокислотной промышленности В книге приведены данные о коррозионной стойкости различных материалов и описаны ...