6.16.1.4. Изохинолины из арилальдегидов и 2,2-диэтоксиэтиламина
Взаимодействие ароматических альдегидов с 2,2-диэтоксиэтиламином приводит к образованию иминов, которые циклизуются в изохинолины, не содержащие заместителей в гетероциклическом фрагменте
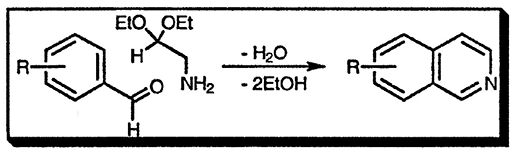
Синтез Померанца-Фрича
Синтез изохинолинов по методу Померанца—Фрича [106] обычно осуществляют в две стадии. На первой стадии проводят конденсацию арилальдегида с 2,2-диэтоксиэтиламином с образованием альдимина. Такая конденсация проходит в мягких условиях и с высоким выходом. На второй стадии альдимин циклизуют под действием сильной кислоты. В условиях циклизации возможен гидролиз имина, что снижает выход продукта циклизации. Лучшие результаты на стадии циклизации достигаются при использовании системы трифторуксусная кислота — трифторид бора [107].
Вторая стадия синтеза Померанца—Фрича аналогична процессам циклизации в синтезах Комба и Скраупа. Первоначальное протонирование способствует отщеплению молекулы этанола и образованию электрофильной частицы, впоследствии атакующей ароматическое кольцо. На заключительной стадии происходит отщепление второй молекулы этанола
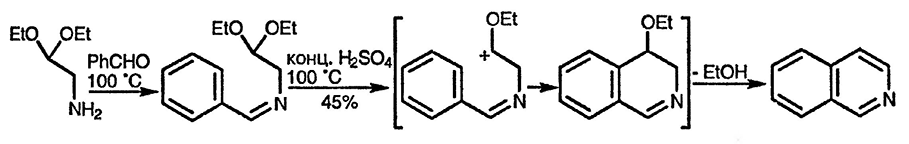
Электрофильный характер циклизации объясняет, почему присутствие в арилальдегиде электронодонорных заместителей (особенно в пара-положении к месту электрофильной атаки, что приводит к изохинолинам, содержащим заместитель в положении 7) обеспечивает лучшее протекание циклизации, а электроноакцепторные заместители затрудняют процесс.
Проблему, связанную с гидролизом иминов в условиях циклизации, можно избежать при использовании субстратов с более низкой степенью окисления и содержащих при атоме азота тозильную группу, которая способна к последующему элиминированию в виде толуолсульфиновой кислоты. Такие субстраты можно получить при восстановлении и последующем тозилировании иминов [108] или при бензилировании натриевой соли N-тозил-2,2-диметоксиэтиламина [109]. Альтернативный подход к таким соединением связан с бензилированием N-тозиламиноацеталя бензиловым спиртом в условиях реакции Мицунобу [110]. Циклизация ацеталя бензиламиноуксусного альдегида под действием хлорсуль-фоновой кислоты представляет собой прямой метод получения ароматических производных изохинолина [111].
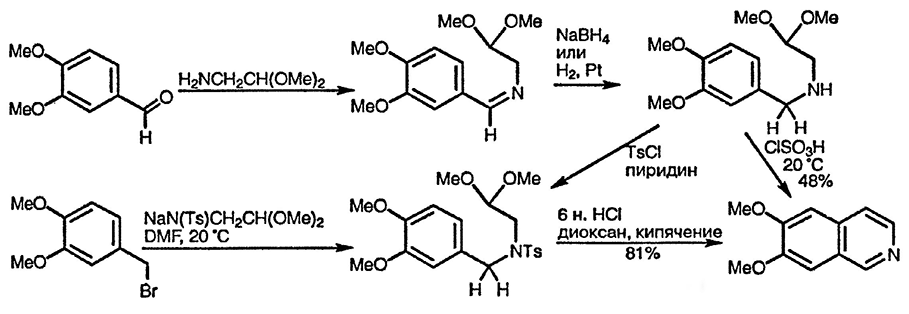
Изохинолины, содержащие заместитель в положении 1, трудно получить при использовании стандартного метода Померанца—Фрича. На первой стадии синтеза таких производных изохинолина необходимо провести конденсацию арил-кетона с ацеталем аминоуксусного альдегида, однако такая реакция идёт менее гладко, чем в случае ароматического альдегида. Для того чтобы избежать затруднения такого рода, предложено использовать конденсацию соответствующего бензиламина с диэтилацеталям глиоксаля для получения изомерного имина и его дальнейшую конденсацию под действием кислоты [112].
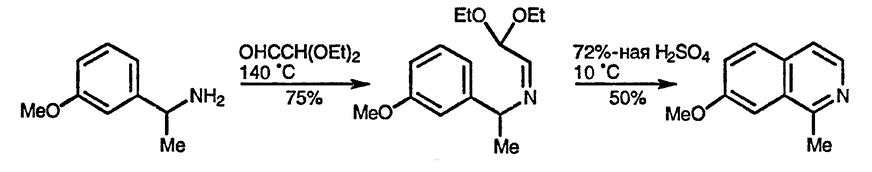
6.16.1.4. Изохинолины из арилальдегидов и 2,2-диэтоксиэтиламина
Список литературы к главе 6
Упражнения к главе 6
Глава 6
- 6. Хинолины и изохинолины: реакции и методы снитеза
- 6.1. Реакции с электрофильными реагентами
- 6.1.1. Присоединение по атому азота
- 6.1.2. Замещение при атоме углерода
- 6.1.2.1. Протонный обмен
- 6.1.2.2. Нитрование
- 6.1.2.3. Сульфирование
- 6.1.2.4. Галогенирование
- 6.1.2.5. Ацилирование и алкилирование
- 6.2. Реакции с окислителями
- 6.3. Реакции с нуклеофильными реагентами
- 6.3.1. Нуклеофильное замещение атома водорода
- 6.3.1.1 Алкилирование и арилирование
- 6.3.1.2. Аминирование и нитрование
- 6.3.2. Гидроксилирование
- 6.3.2.1. Нуклеофильное замещение атома галогена
- 6.4. Реакции с основаниями
- 6.4.1. Депротонирование при атоме углерода
- 6.5. Реакции C-металлированных хинолинов и изохинолинов
- 6.5.1. Литийорганические производные
- 6.5.2. Цинкорганические соединения
- 6.5.3. Реакции, катализируемые палладием и никелем
- 6.6. Реакции со свободными радикалами
- 6.7. Реакции с восстановителями
- 6.8. Электроциклические реакции основного состояния
- 6.9. Фотохимические реакции
- 6.10. Оксихинолины и оксиизохинолины
- 6.11. Аминохинолины и аминоизохинолины
- 6.12. Алкилхинолины и алкилизохинолины
- 6.13. Хинолин- и изохинолинкарбоновые кислоты и их эфиры
- 6.14. Четвертичные хинолиниевые и изохинолиниевые соли
- 6.15. N-оксиды хинолина и изохинолина
- 6.16. Методы синтеза хинолинов и изохинолинов
- 6.16.1. Синтез кольца
- 6.16.1.1. Хинолины из ариламинов и 1,3-дикарбонильных соединений
- 6.16.1.2. Хинолины из ариламинов и α,β-ненасыщенных карбонильных соединений
- 6.16.1.3. Хинолины из орто-ацилариламинов и карбонильных соединений
- 6.16.1.4. Изохинолины из арилальдегидов и 2,2-диэтоксиэтиламина
- 6.16.1.5. Изохинолины из арилэтиламидов
- 6.16.1.6. Изохинолины из активированных арилэтиламинов и альдегидов
- 6.16.1.7. Современные методы
- 6.16.2. Примеры синтезов некоторых важных производных хинолина и изохинолина
- 6.16.2.1. Хлорохин
- 6.16.2.2. Папаверин
- 6.16.2.3. Метоксатин
Дополнительно:
Книга представляет собой материалы XVII Международного конгресса по теоретической ...
 Химия и технология полиформальдегида
Химия и технология полиформальдегида Книга посвящена изложению теоретических основ синтеза нового полимерного ...
 Основные процессы переработки полимеров (теория и методы расчёта)
Основные процессы переработки полимеров (теория и методы расчёта) В книге систематизированы современные представления в области реологии ...
 Неорганические препараты
Неорганические препараты Руководство к препаративному практикуму для студентов, начинающих изучение ...