6.3.2.1. Нуклеофильное замещение атома галогена
Для реакций этого типа действует общий принцип — реакционная способность атомов галогена в бензольных кольцах хинолина и изохинолина в положении C(3) хинолина и C(4) изохинолина аналогична реакционной способности галогенобензолов. В то же время для атомов галогена в положениях 2 и 4 хинолина и положении 4 изохинолина характерны те же реакции с нуклеофильными реагентами, что и для α- и γ-галогенопиридинов (см. разд. 5.3.2.). 3-Галогеноизохинолины по своей реакционной способности занимают промежуточное положение [24].
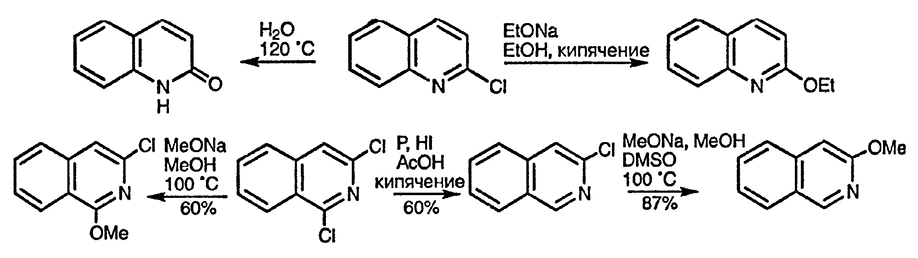
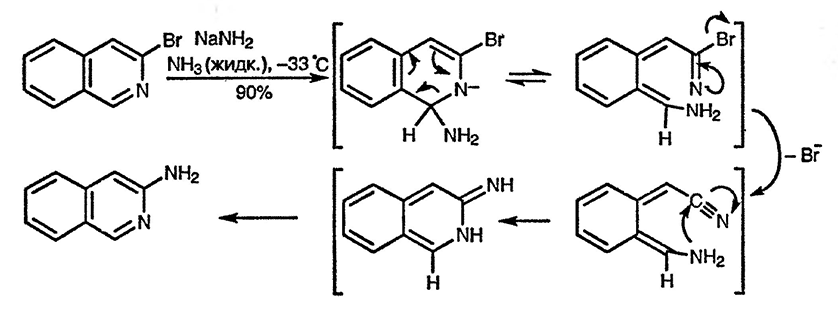
Особый случай — реакция относительно мало реакционноспособного 3-бромизохинолина с амидом натрия. В данном случае реализуется механизм ANRORC (Addition of Nucleophile, Ring Opening and Ring Closure присоединение нуклеофила, раскрытие цикла и замыкание цикла), что приводит к продукту прямого замещения атома брома на аминогруппу, однако в аминогруппе оказывается атом азота, локализованный прежде в изохинолиновом цикле [25].
Глава 6
- 6. Хинолины и изохинолины: реакции и методы снитеза
- 6.1. Реакции с электрофильными реагентами
- 6.1.1. Присоединение по атому азота
- 6.1.2. Замещение при атоме углерода
- 6.1.2.1. Протонный обмен
- 6.1.2.2. Нитрование
- 6.1.2.3. Сульфирование
- 6.1.2.4. Галогенирование
- 6.1.2.5. Ацилирование и алкилирование
- 6.2. Реакции с окислителями
- 6.3. Реакции с нуклеофильными реагентами
- 6.3.1. Нуклеофильное замещение атома водорода
- 6.3.1.1 Алкилирование и арилирование
- 6.3.1.2. Аминирование и нитрование
- 6.3.2. Гидроксилирование
- 6.3.2.1. Нуклеофильное замещение атома галогена
- 6.4. Реакции с основаниями
- 6.4.1. Депротонирование при атоме углерода
- 6.5. Реакции C-металлированных хинолинов и изохинолинов
- 6.5.1. Литийорганические производные
- 6.5.2. Цинкорганические соединения
- 6.5.3. Реакции, катализируемые палладием и никелем
- 6.6. Реакции со свободными радикалами
- 6.7. Реакции с восстановителями
- 6.8. Электроциклические реакции основного состояния
- 6.9. Фотохимические реакции
- 6.10. Оксихинолины и оксиизохинолины
- 6.11. Аминохинолины и аминоизохинолины
- 6.12. Алкилхинолины и алкилизохинолины
- 6.13. Хинолин- и изохинолинкарбоновые кислоты и их эфиры
- 6.14. Четвертичные хинолиниевые и изохинолиниевые соли
- 6.15. N-оксиды хинолина и изохинолина
- 6.16. Методы синтеза хинолинов и изохинолинов
- 6.16.1. Синтез кольца
- 6.16.1.1. Хинолины из ариламинов и 1,3-дикарбонильных соединений
- 6.16.1.2. Хинолины из ариламинов и α,β-ненасыщенных карбонильных соединений
- 6.16.1.3. Хинолины из орто-ацилариламинов и карбонильных соединений
- 6.16.1.4. Изохинолины из арилальдегидов и 2,2-диэтоксиэтиламина
- 6.16.1.5. Изохинолины из арилэтиламидов
- 6.16.1.6. Изохинолины из активированных арилэтиламинов и альдегидов
- 6.16.1.7. Современные методы
- 6.16.2. Примеры синтезов некоторых важных производных хинолина и изохинолина
- 6.16.2.1. Хлорохин
- 6.16.2.2. Папаверин
- 6.16.2.3. Метоксатин
Дополнительно:
 Курс технической химии
Курс технической химии Хозяйственные и технические руководства, издаваемые от императорского вольного ...
Во втором издании (1-е издание вышло в 1983 г.) рассмотрены вопросы электронного ...
Книга представляет собой краткое руководство по технологии переработки ...