6.14. Четвертичные хинолиниевые и изохинолиниевые соли
Самое важное свойство четвертичных хинолиниевых и изохинолиниевых солей заключается в лёгком присоединении к ним нуклеофильных агентов по положению 2 в хинолиниевом катионе и по положению 1 в изохинолиниевом катионе. Гидроксид-ион, гидрид-ион [69] и металлоорганические соединения легко присоединяются с образованием дигидроароматических аддуктов, которые требуют чрезвычайно тщательного обращения, поскольку склонны к диспропорционированию (см. также разд. 6.7.) и окислению [70].
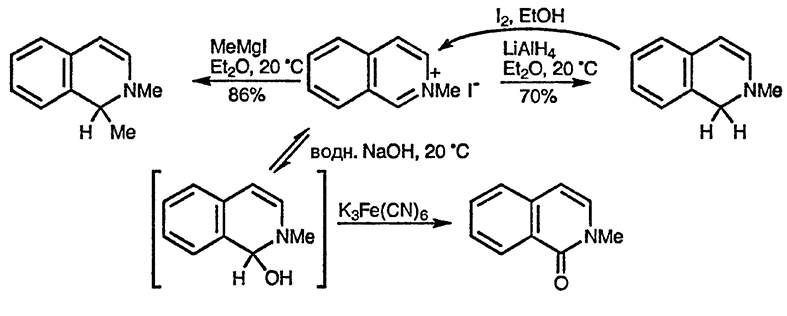
Наиболее легко присоединение нуклеофильных агентов идёт по положению 2 хинолиниевого катиона, при обратимости реакции возможно образование термодинамически более стабильного продукта присоединения по положению 4 вследствие наличия двойной связи, сопряжённой с атомом азота [71]. Присоединить еноляты кетонов по положению 2 хинолиниевых солей можно при ультразвуковом облучении [72].
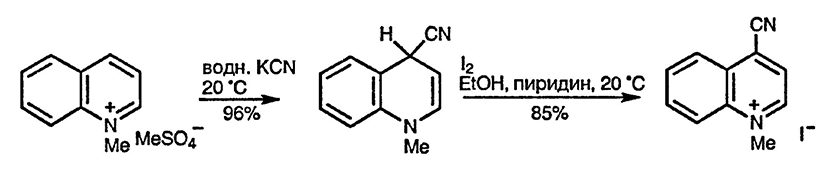
Взаимодействие хинолина и изохинолина с боргидридом натрия в присутствии смеси уксусной кислоты и уксусного ангидрида представляет собой удобный способ получения N-ацетил-1,2-дигидропроизводных [73].
Давно известная реакция Рейссерта — это кинетически контролируемое присоединение цианид-иона к N+-ацилхинолиниевым и N+-ацилизохинолиниевым солям, в классическом варианте [74] ацилирующим агентом служит бензоилхлорид. Соединения Рейссерта [75] обычно получают в двухфазной системе дихлорметан вода; разработанные в последнее время способы оптимизации процесса связаны с использованием катализаторов межфазного переноса, а также ультразвукового облучения [76] и краун-эфиров [77].
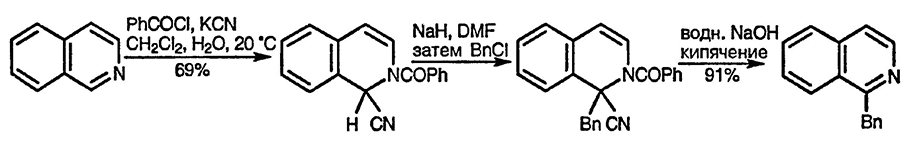
Соединения Рейссерта широко используются для получения производных хинолина и изохинолина: например, депротонирование, алкилирование и удаление ацильной группы и цианогруппы приводит к замещённым гетероциклическим соединениям. N-Сульфонильные аналоги соединений Рейссерта легко отщепляют арилсульфинатную группу, что используется для введения цианогруппы в хинолин и изохинолин [78].
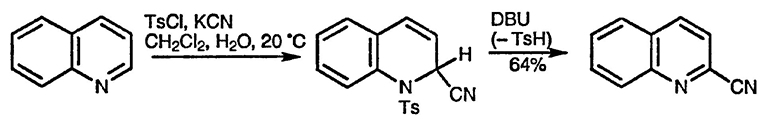
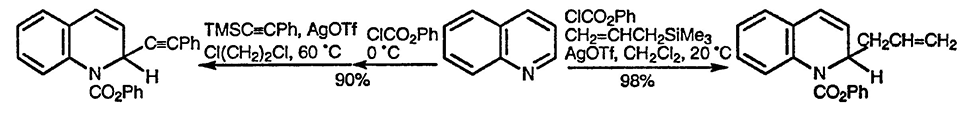
Аллилсиланы также могут взаимодействовать с N-ацилизохинолиниевыми [79] и N-ацилхинолиниевыми [80] солями; возможно присоединение также силилалкенов [81] при катализе ионами серебра.
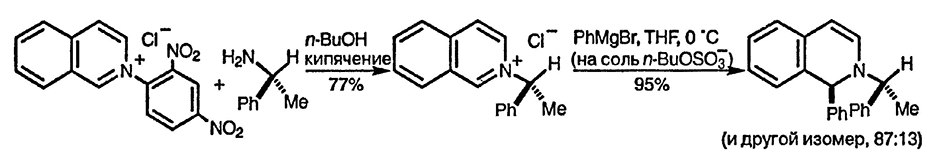
Соли Цинке изохинолинового рада [82] легко превращаются в хиральные изохинолиниевые соли при реакции с хиральными аминами [83]. Нуклеофильное присоединение к таким солям отличается хорошей стереоселективностью [84].
6.14. Четвертичные хинолиниевые и изохинолиниевые соли
Список литературы к главе 6
Упражнения к главе 6
Глава 6
- 6. Хинолины и изохинолины: реакции и методы снитеза
- 6.1. Реакции с электрофильными реагентами
- 6.1.1. Присоединение по атому азота
- 6.1.2. Замещение при атоме углерода
- 6.1.2.1. Протонный обмен
- 6.1.2.2. Нитрование
- 6.1.2.3. Сульфирование
- 6.1.2.4. Галогенирование
- 6.1.2.5. Ацилирование и алкилирование
- 6.2. Реакции с окислителями
- 6.3. Реакции с нуклеофильными реагентами
- 6.3.1. Нуклеофильное замещение атома водорода
- 6.3.1.1 Алкилирование и арилирование
- 6.3.1.2. Аминирование и нитрование
- 6.3.2. Гидроксилирование
- 6.3.2.1. Нуклеофильное замещение атома галогена
- 6.4. Реакции с основаниями
- 6.4.1. Депротонирование при атоме углерода
- 6.5. Реакции C-металлированных хинолинов и изохинолинов
- 6.5.1. Литийорганические производные
- 6.5.2. Цинкорганические соединения
- 6.5.3. Реакции, катализируемые палладием и никелем
- 6.6. Реакции со свободными радикалами
- 6.7. Реакции с восстановителями
- 6.8. Электроциклические реакции основного состояния
- 6.9. Фотохимические реакции
- 6.10. Оксихинолины и оксиизохинолины
- 6.11. Аминохинолины и аминоизохинолины
- 6.12. Алкилхинолины и алкилизохинолины
- 6.13. Хинолин- и изохинолинкарбоновые кислоты и их эфиры
- 6.14. Четвертичные хинолиниевые и изохинолиниевые соли
- 6.15. N-оксиды хинолина и изохинолина
- 6.16. Методы синтеза хинолинов и изохинолинов
- 6.16.1. Синтез кольца
- 6.16.1.1. Хинолины из ариламинов и 1,3-дикарбонильных соединений
- 6.16.1.2. Хинолины из ариламинов и α,β-ненасыщенных карбонильных соединений
- 6.16.1.3. Хинолины из орто-ацилариламинов и карбонильных соединений
- 6.16.1.4. Изохинолины из арилальдегидов и 2,2-диэтоксиэтиламина
- 6.16.1.5. Изохинолины из арилэтиламидов
- 6.16.1.6. Изохинолины из активированных арилэтиламинов и альдегидов
- 6.16.1.7. Современные методы
- 6.16.2. Примеры синтезов некоторых важных производных хинолина и изохинолина
- 6.16.2.1. Хлорохин
- 6.16.2.2. Папаверин
- 6.16.2.3. Метоксатин
Дополнительно:
 Естествознание и проблема белка. Химическое и пространственное строение белков. Структурная организация белков
Естествознание и проблема белка. Химическое и пространственное строение белков. Структурная организация белков В книге прослежены этапы развития исследований химического и пространственного ...
 О стекловидном состоянии вещества
О стекловидном состоянии вещества Воспроизведено в оригинальной авторской орфографии издания 1929 года ...
 Полиуретановые эластомеры
Полиуретановые эластомеры В книге изложены вопросы, связанные с получением и применением сравнительно ...
 Энантиомерно чистые небелковые аминокислоты. Способы получения
Энантиомерно чистые небелковые аминокислоты. Способы получения Первая в отечественной литературе монография, посвящённая небелковым ...