6.16.1.2. Хинолины из ариламинов и α,β-ненасыщенных карбонильных соединений
Взаимодействие ариламинов с α,β-ненасыгценными карбонильными соединениями в присутствии окислителей приводит к образованию хинолинов. Использование глицерина для получения акролеина in situ позволяет получить хинолин, не содержащий заместителей в гетероциклическом фрагменте.
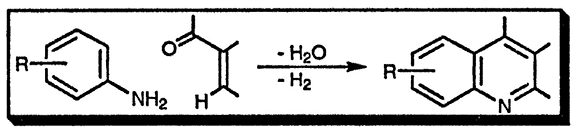
Синтез Скраупа [96]
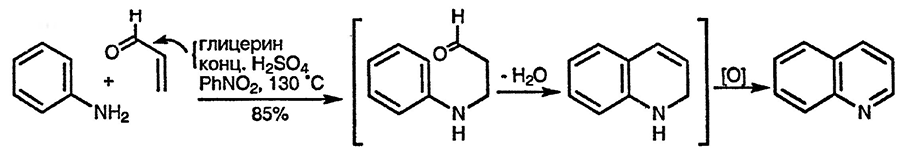
Нагревание смеси анилина, концентрированной серной кислота, глицерина и мягкого окисляющего агента приводит в результате необычной реакции к образованию хинолина [97]. Как было показано, при этом происходит дегидратация глицерина, приводящая к образованию акролеина, затем анилин присоединяется к акролеину по типу сопряжённого присоединения. В дальнейшем происходит катализируемая кислотой циклизация с образованием 1,2-дигидрохинолина. Окисление на заключительном этапе приводит к ароматической структуре. В классическом варианте в качестве окислителя используется нитробензол или мышьяковая кислота; введение в реакционную смесь небольшого количества иодида натрия позволяет серной кислоте выступать в роли окислителя [12]. Синтез Скраупа наиболее пригоден для получения не замещённых по гетероциклу хинолинов [98].
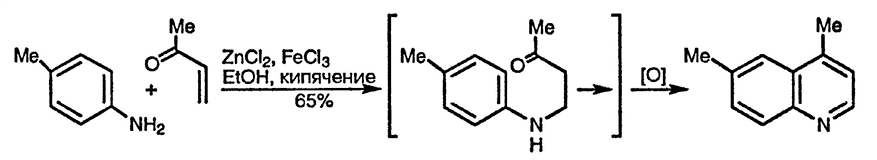
При использование замещённых карбонильных компонентов были получены подтверждения описанного выше механизма и доказано, что на первой стадии реализуется именно сопряжённое присоединение анилина к непредельному карбонильному соединению, а не взаимодействие анилина с карбонильной труппой.
В некоторых случаях образование хинолинов по методу Скраупа проходит очень бурно и необходимо предпринимать меры для предотвращения такого течения реакции. Использование предварительно полученного продукта сопряжённого присоединения и других окислителей (наилучшие результаты даёт применение n-хлоранила) характеризуется рядом преимуществ в плане как выхода целевых соединений, так и контроля за ходом реакции [99].
Ориентация процесса замыкания цикла при синтезе Скраупа
При использовании в синтезе Скраупа мета-замещённых анилинов возможно образование двух изомерных хинолинов, содержащих заместители в положении 5 или 7. При наличии электронодонорных заместителей в мета-положении анилина замыкание цикла проходит по пара-положению, что приводит к образованию преимущественно 7-замещенных хинолинов; так, применение в синтезе Скраупа мета-галогенозамещенных анилинов приводит к 7-галогенозаме-щенным хинолинам. Ариламины, содержащие в мета-положении сильные электроноакцепторные заместители, превращаются в условиях синтеза Скраупа главным образом в 5-замещенные хинолины.
6.16.1.2. Хинолины из ариламинов и α,β-ненасыщенных карбонильных соединений
Список литературы к главе 6
Упражнения к главе 6
Глава 6
- 6. Хинолины и изохинолины: реакции и методы снитеза
- 6.1. Реакции с электрофильными реагентами
- 6.1.1. Присоединение по атому азота
- 6.1.2. Замещение при атоме углерода
- 6.1.2.1. Протонный обмен
- 6.1.2.2. Нитрование
- 6.1.2.3. Сульфирование
- 6.1.2.4. Галогенирование
- 6.1.2.5. Ацилирование и алкилирование
- 6.2. Реакции с окислителями
- 6.3. Реакции с нуклеофильными реагентами
- 6.3.1. Нуклеофильное замещение атома водорода
- 6.3.1.1 Алкилирование и арилирование
- 6.3.1.2. Аминирование и нитрование
- 6.3.2. Гидроксилирование
- 6.3.2.1. Нуклеофильное замещение атома галогена
- 6.4. Реакции с основаниями
- 6.4.1. Депротонирование при атоме углерода
- 6.5. Реакции C-металлированных хинолинов и изохинолинов
- 6.5.1. Литийорганические производные
- 6.5.2. Цинкорганические соединения
- 6.5.3. Реакции, катализируемые палладием и никелем
- 6.6. Реакции со свободными радикалами
- 6.7. Реакции с восстановителями
- 6.8. Электроциклические реакции основного состояния
- 6.9. Фотохимические реакции
- 6.10. Оксихинолины и оксиизохинолины
- 6.11. Аминохинолины и аминоизохинолины
- 6.12. Алкилхинолины и алкилизохинолины
- 6.13. Хинолин- и изохинолинкарбоновые кислоты и их эфиры
- 6.14. Четвертичные хинолиниевые и изохинолиниевые соли
- 6.15. N-оксиды хинолина и изохинолина
- 6.16. Методы синтеза хинолинов и изохинолинов
- 6.16.1. Синтез кольца
- 6.16.1.1. Хинолины из ариламинов и 1,3-дикарбонильных соединений
- 6.16.1.2. Хинолины из ариламинов и α,β-ненасыщенных карбонильных соединений
- 6.16.1.3. Хинолины из орто-ацилариламинов и карбонильных соединений
- 6.16.1.4. Изохинолины из арилальдегидов и 2,2-диэтоксиэтиламина
- 6.16.1.5. Изохинолины из арилэтиламидов
- 6.16.1.6. Изохинолины из активированных арилэтиламинов и альдегидов
- 6.16.1.7. Современные методы
- 6.16.2. Примеры синтезов некоторых важных производных хинолина и изохинолина
- 6.16.2.1. Хлорохин
- 6.16.2.2. Папаверин
- 6.16.2.3. Метоксатин
Дополнительно:
Книга представляет собой краткое руководство по технологии переработки ...
 Теория углового момента
Теория углового момента Книга учёного из США относится к новому направлению в химии — динамической ...
Рассмотрено современное состояние проблемы радикальной полимеризации виниловых ...
 О водном бромокуприте лития
О водном бромокуприте лития Воспроизведено в оригинальной авторской орфографии издания 1898 года ...