24.10.2.3. Диазотирование
Взаимодействие 2-амино- и 6-аминопуринов с азотистой кислотой происходит точно также, как для 2-аминопиридинов — в результате образуются соли диазония, но менее стабильные, чем фенидциазониевые соли. Несмотря на это, их можно использовать для введения таких групп, как галогены [81], или, безусловно, кислорода при взаимодействии с водой с потерей атома азота. Значительно более устойчивы 8-диазониевые соли [82].

Диазотирование можно также проводить в растворах оснований, особенно в случае чувствительных к кислотам рибозидов [83]. Нуклеофильное замещение аминогруппы на гидроксигруппу можно осуществить ферментативно в присутствии аденозиндезаминазы; это полезный препаративный метод, так как он позволяет проводить очень селективную трансформацию в очень мягких условиях [84]. Химический гидролиз требует более жёстких условий.
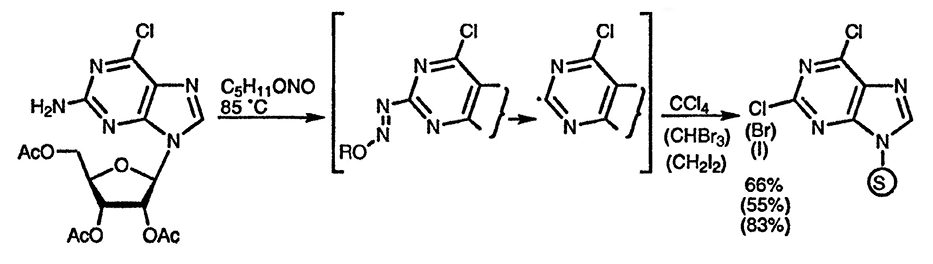
В подобной реакции с алкилнитритами образуются пуринил-радикалы, которые способны отщеплять атом галогена от галогеносодержащего растворителя, и такой метод обычно предпочтителен для превращения аминопуринов в галогенопурины [85]. Аналогично при использовании диметилсульфида образуются метилтиопурины [86].
Глава 24
- 24. Пурины: реакции и методы синтеза
- 24.1. Нуклеиновые кислоты, нуклеозиды и нуклеотиды
- 24.2. Реакции с электрофильными реагентами
- 24.2.1. Присоединение по атому азота
- 24.2.1.1. Протонирование
- 24.2.1.2. Алкилирование по атому азота
- 24.2.1.3. Ацилирование по атому азота
- 24.2.1.4. Окисление по атому азота
- 24.2.2. Замещение по атому углерода
- 24.2.2.1. Галогенирование
- 24.2.2.2. Нитрование
- 24.2.2.3. Реакции сочетания с солями диазония
- 24.3. Реакции со свободными радикалами
- 24.4. Реакции с окислителями
- 24.5. Реакции с восстановителями
- 24.6. Реакции с нуклеофильными реагентами
- 24.7. Реакции с основаниями
- 24.7.1. Депротонирование N-водорода
- 24.7.2. Депротонирование С-водорода
- 24.8. Реакции N-металлированных пуринов
- 24.9. Реакции C-металлированных пуринов
- 24.9.1. Литийорганические производные
- 24.9.2. Реакции, катализируемые палладием
- 24.10. Окси- и аминопурины
- 24.10.1. Оксипурины
- 24.10.1.1. Алкилирование
- 24.10.1.2. Ацилирование
- 24.10.1.3. Замещение на атом хлора
- 24.10.1.4. Замещение на атом серы
- 24.10.2. Аминопурины
- 24.10.2.1. Алкилирование
- 24.10.2.2. Ацилирование
- 24.10.2.3. Диазотирование
- 24.10.3. Тиопурины
- 24.11. Алкилпурины
- 24.12. Пуринкарбоновые кислоты
- 24.13. Синтезы пуринов
- 24.13.1. Синтез кольца
- 24.13.1.1. Из 4,5-диаминопиримидинов
- 24.13.1.2. Из 5-аминоимидазол-4-карбоксамида или 5-аминоимидазол-4-карбонитрила
- 24.13.1.3. Реакцией циклоприсоединения
- 24.13.1.4. Синтезы «в одной колбе»
- 24.13.2. Примеры синтезов некоторых важных пуринов
- 24.13.2.1. Аристеромицин
- 24.13.2.2. Аденозин
- 24.12.2.3. Силденафил (Виагра)
Дополнительно:
 Химические методы исследования синтетических смол и пластических масс
Химические методы исследования синтетических смол и пластических масс В книге описаны химические методы исследования синтетических смол и ...
 Поверхностно-активные вещества. Синтез, свойства, анализ, применение
Поверхностно-активные вещества. Синтез, свойства, анализ, применение Приведена современная классификация ПАВ и их смесей, рассмотрены технологии ...
