15.5.1. Литийорганические производные
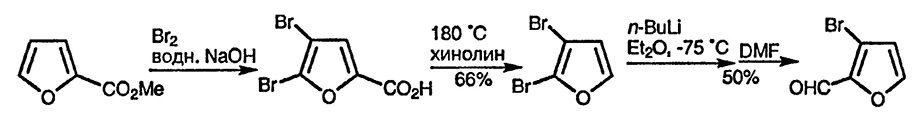
Металлирование по положению 3 может быть достигнуто путём обмена металл/галоген. Большая стабильность α-карбаниона проявляется в селективном монообмене в 2,3-дибромфуране атома брома в α-положении [28] [54].
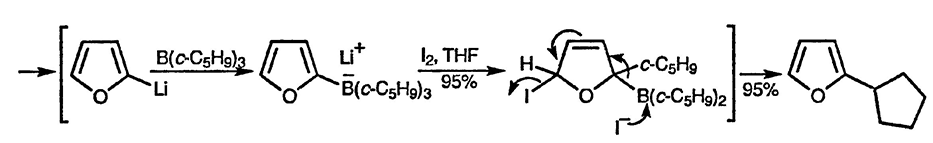
Существует множество примеров использования 2- и 3-литийфуранов в реакциях с разнообразными электрофильными реагентами, такими, как альдегиды и кетоны [42] [55], а также галогениды [56]. Было показано, что при обработке 2-литийфурана хлоридом меди(II) образуется 2,2’-бифуран [57], а при взаимодействии с триал-килборанами получают бораты, дальнейшая обработка которых галогенами служит прекрасным методом введения алкильных групп в α-положение фурана [58].
Взаимодействие 3-литийфурана, наилучшим образом получаемого [59] из 3-бромфурана, с бис(триметилсилил)пероксидом позволяет напрямую синтезировать триметилсилиловый эфир 3-гидроксифурана [60]. Окислением эфиров 2-боронатов получают 2-бутенолиды (разд. 15.12.1.) [61]. Фуран-2- и фуран-3-борные кислоты синтезируют путём взаимодействия соответствующих литиированных производных с трибутилборатом обычным способом [62].
Глава 15
- 15. Фураны: реакции и методы синтеза
- 15.1. Реакции с электрофильными реагентами
- 15.1.1. Протонирование
- 15.1.1.1. Реакции протонированных фуранов
- 15.1.2. Нитрование
- 15.1.3. Сульфирование
- 15.1.4. Галогенирование
- 15.1.5. Ацилирование
- 15.1.6. Алкилирование
- 15.1.7. Конденсация с альдегидами и кетонами
- 15.1.8. Конденсация с иминами и иминиевыми солями
- 15.1.9. Меркурирование
- 15.2. Реакции с окислителями
- 15.3. Реакции с нуклеофильными реагентами
- 15.4. Реакции с основаниями
- 15.4.1. Депротонирование C-водорода
- 15.5. Реакции C-металлированных фуранов
- 15.5.1. Литийорганические производные
- 15.5.2. Реакции сочетания, катализируемые палладием
- 15.6. Реакции со свободными радикалами
- 15.7. Реакции с восстановителями
- 15.8. Электроциклические реакции (основного состояния)
- 15.9. Фотохимические реакции
- 15.10. C-X-производные фурана; реакции с участием заместителей
- 15.11. Фуранкарбоновые кислоты и их эфиры
- 15.12. Окси- и аминофураны
- 15.12.1. Оксифураны
- 15.12.2. Аминофураны
- 15.13. Синтезы фуранов
- 15.13.1. Синтез кольца
- 15.13.1.1. Из 1,4-дикарбонильных соединений
- 15.13.1.2. Из γ-гидрокси-α,β-ненасыщенных карбонильных соединений
- 15.13.1.3. Из алленилкетонов
- 15.13.1.4. Из α-галогенокарбонильных и 1,3-дикарбонильных соединений
- 15.13.1.5. Другие методы
- 15.13.2. Примеры синтезов некоторых важных производных фурана
- 15.13.2.1. Трис(фуранил)-18-краун-6
- 15.13.2.2. Фуранеол
- 15.13.2.3. Ранитидин
Дополнительно:
 Химические волокна. Словарь-справочник
Химические волокна. Словарь-справочник В словаре приводятся в алфавитном порядке русские и иностранные торговые и ...
В справочник включены сведения об органических стабилизаторах, ускорителях и ...
В работе описывается использование квантовомеханических методов (вариационного, ...
 Химия в нашем доме
Химия в нашем доме Описаны самые разнообразные химические средства, применяемые в быту для стирки, ...