21.9. Электроциклические реакции
Оксазолы легко вступают в реакции циклоприсоединения по положениям 2 и 5 аналогично фуранам (разд. 15.8.), тиазолы реагируют с алкинами подобным же образом (например, см. разд. 14.13.1.7.), однако существует только один пример такого циклоприсоединения в химии имидазола. Тиазол и имидазол реагируют с высокоэлектрофильными алкинами через первоначальное электрофильное присоединение по атому азота с последующей внутримолекулярной нуклеофильной циклизацией [93].
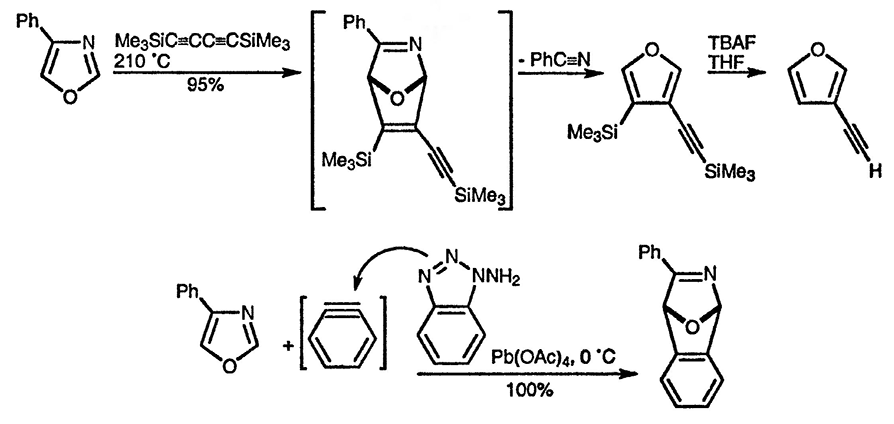
Известны реакции циклоприсоединения оксазола с алкиновыми диенофилами (последовательно идущие реакции Дильса-Альдера, ретро-Дильса-Альдера и потеря нитрила приводят к образованию фуранов), с дегидробензолом (первичный аддукт может быть выделен) [95] и типичными алкеновыми диенофилами. Первичные аддукты присоединения синглетного кислорода перегруппировываются по недостаточно установленному механизму в триамиды, которые широко используются в органическом синтезе [96]. Что касается имидазола, существует только один пример внутримолекулярного взаимодействия, в результате которого после потери циановодорода образуется пиррол [97].
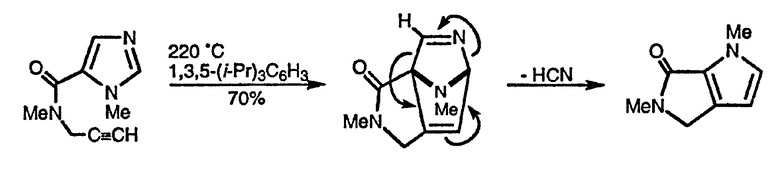
Особое внимание уделяется реакциям оксазола с типичными диенофилами Дильса-Альдера [98]. Аддукты могут быть превращены в пиридины другими способами (разд. 5.15.1.4.). Наличие электронодонорных заместителей в оксазолах увеличивает скорость реакции: 5-алкоксиоксазолы сравнимы по реакционной способности с типичными полностью углеродными диенами. Особенно полезные диенофилы — N-ацилоксазолоны — используют в качестве синтонов для получения цис-1,2-аминоспиртов [99].
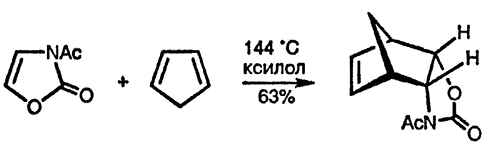
Термически индуцируемая перегруппировка оксазол-4-альдегидов, оксазол-4-кетонов [100] и 5-этокси-4-амидов [101] происходит при достаточно низких температурах (90-120 °C) с образованием более стабильных карбонильных соединений. В качестве интермедиатов, как полагают, образуются нитрилий-еноляты
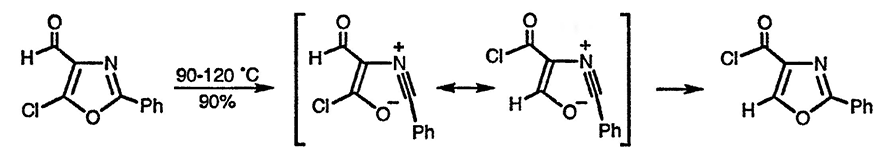
Отдельные примеры участия 1,3-азолов в качестве 2π-компонент в процессах ииклоприсоединения включают реакцию 4-нитро-2-фенилоксазола с диенами по связи 4,5 [102] и внутримолекулярное циклоприсоединение, показанное ниже на примере имидазола, которое включает взаимодействие с электронодефицитным диеном и завершается потерей циановодорода [103]
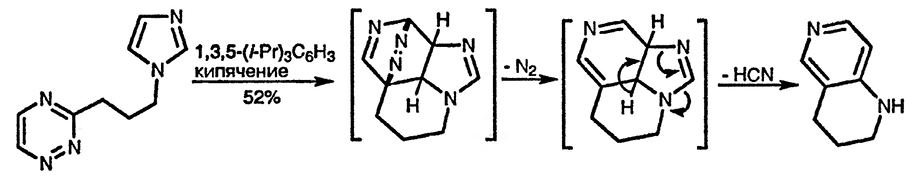
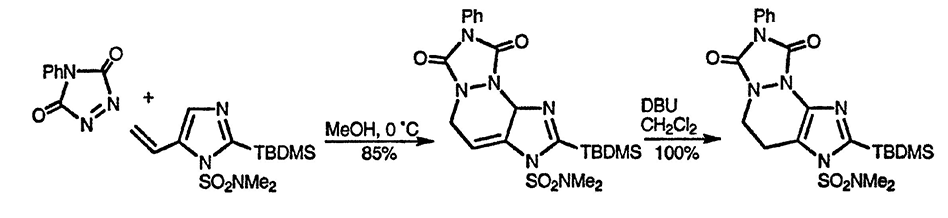
При наличии сильной электроноакцепторной группы у атома азота (но гораздо менее эффективной, чем, например, метоксиметильная) 5-винилимидазол может участвовать в реакции циклоприсоединения в качестве 4π-компонента, как показано ниже [104]:
Глава 21
- 21. 1,3-азолы — имидазолы, тиазолы и оксазолы: реакции и методы синтеза
- 21.1. Реакции с электрофильными реагентами
- 21.1.1. Присоединение по атому азота
- 21.1.1.1.1. Протонирование
- 21.1.1.2. Алкилирование по атому азота
- 21.1.1.3. Ацилирование по атому азота
- 21.1.2. Замещение по атому углерода
- 21.1.2.1. Протонирование
- 21.1.2.2. Нитрование
- 21.1.2.3. Сульфирование
- 21.1.2.4. Галогенирование
- 21.1.2.5. Ацилирование
- 21.1.2.6. Реакции с альдегидами
- 21.1.2.7. Реакции с иминиевыми солями
- 21.2. Реакции с окислителями
- 21.3. Реакции с нуклеофильными реагентами
- 21.3.1. Реакции с раскрытием цикла
- 21.3.2. Реакции замещения атома галогена
- 21.4. Реакции с основаниями
- 21.4.1. Депротонирование группы NH
- 21.4.2. Депротонирование СН
- 21.5. Реакции N-металлированных имидазолов
- 21.6. Реакции C-металлированных 1,3-азолов
- 21.6.1. Литийорганические производные
- 21.6.2. Реакции, катализируемые палладием
- 21.7. Реакции со свободными радикалами
- 21.8. Реакции с восстановителями
- 21.9. Электроциклические реакции
- 21.10. Алкил-1,3-азолы
- 21.11. Четвертичные соли 1,3-азолов
- 21.12. Гидрокси- и амино-1,3-азолы
- 21.13. N-оксиды 1,3-азолов
- 21.14. Синтезы 1,3-азолов
- 21.14.1. Синтез кольца
- 21.14.1.1. Из α-галогенокарбонильных соединений (или их эквивалентов) и трёхатомного фрагмента, поставляющего два гетероатома и атом C(2) кольца
- 21.14.1.2. Циклодегидратацией α-ациламинокарбонильных соединений
- 21.14.1.3. Из изонитрилов
- 21.14.1.4. Оксазолы из α-диазокарбонильных соединений
- 21.14.1.5. Дегидрированием
- 21.14.2. Примеры некоторых важных синтезов с участием 1,3-азолов
- 21.14.2.1. 4(5)-Фторгистамин
- 21.14.2.2. Пиридоксин
- 21.14.2.3. Тиамин
- 21.14.2.4. Тиено[2,3-d]имидазол
- 21.14.2.5. Гроссуларин-2
Дополнительно:
 Книга для чтения по неорганической химии (комплект из 2 книг)
Книга для чтения по неорганической химии (комплект из 2 книг) Перед вами третье издание «Книги для чтения по неорганической химии». Эта книга ...
Книга посвящена получению, переработке и применению полистирола — ...
Настоящий англо-русский словарь по каучуку, резине и химическим волокнам ...
В книге рассматриваются основы методов определения геометрического строения ...