5.10.3.1. Электрофильное присоединение и замещение
Все изомерные аминопиридины проявляют основные свойства в большей степени, чем незамещённый пиридин, и образуют при протоноровании по кольцевому атому азота кристаллические соли. Производные пиридина с аминогруппами в α- и γ-положениях моноосновны, поскольку положительный заряд делокализуется между двумя атомами азота, как в случае амидиниевого катиона, что препятствует повторному протонированию. Делокализация положительного заряда проявляется значительно в большей степени в 4-аминопиридине (рКа 9,1), чем в 2-изомере (рKa 7,2). В случае β-изомера делокализация невозможна, и в сильнокислых средах 3-аминопиридин способен дважды протонироваться с образованием дикатиона (pKa 6,6 и —1,5) [157].
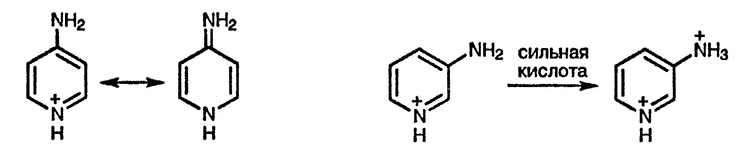
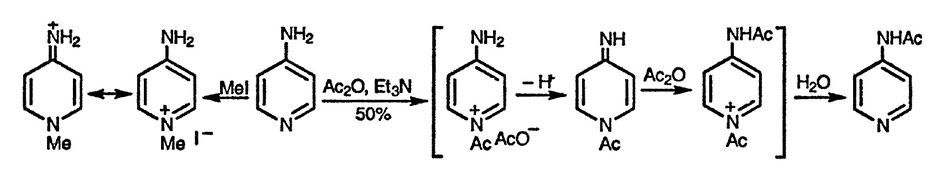
Алкилирование аминопиридинов представляет собой необратимый при комнатной температуре процесс, который приводит к кинетически контролируемому продукту реакции по кольцевому атому азота. [158]. В противоположность этому ацилирование проходит по боковой аминогруппе. Ацетиламинопиридин, вероятно, образуется в результате ряда последовательных процессов — депротонирования аминогруппы N-ациламинопиридиниевой соли, ацилирования аминогруппы и гидролитического удаления ацильной группы от кольцевого атома азота при обработке реакционной смеси водой.
Как и производные бензола, электронодонорные заместители в которых облегчают электрофильное замещение, 2-аминопиридин бромируется в положение 5 в уксусной кислоте даже при комнатной температуре, причём продукт бромирования нитруется также при комнатной температуре с образованием 2-амино-5-бром-3-нитропиридина [159]. Хлорирование 3-аминопиридина приводит к 3-амино-2-хлорпиридину [160]. Нитрование аминопиридинов в кислых средах также идёт относительно легко и для 2- и 4-изомеров проходит селективно по β-положению. Изучение процесса нитрования диалкиламинопиридинов показало, что нитрованию подвергается протонироанный пиридин [161].
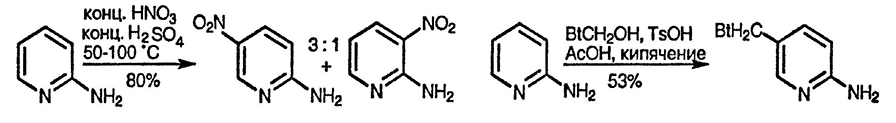
Ранее сообщалось о возможности С-алкилирования аминопиридинов в очень жёстких условиях. В значительно более мягких условиях проходит алкилирование 2-аминопиридина при его взаимодействии с 1-гидроксиметилбензотриазолом (разд. 26.3.) в присутствии кислоты. Следует принять во внимание, что такое C-алкилирование возможно только при обратимости алкилирования по кольцевому атому азота [162]. Образующийся при таком алкилировании продукт реакции обладает всеми свойствами производных бензотриазолов, что чрезвычайно полезно при дальнейших синтетических превращениях (разд. 26.3.).
Глава 5
- 5. Пиридины: реакции и методы синтеза
- 5.1. Реакции с электрофильными реагентами
- 5.1.1. Присоединение к атому азота
- 5.1.1.1. Протонирование атома азота
- 5.1.1.2. Нитрование по атому азота
- 5.1.1.3. Аминирование по атому азота
- 5.1.1.4. Окисление атома азота
- 5.1.1.5. Сульфирование по атому азота
- 5.1.1.6. Галогенирование по атому азота
- 5.1.1.7. Ацилирование по атому азота
- 5.1.1.8. Алкилирование по атому азота
- 5.1.1.9. Реакции комплексообразования
- 5.1.2. Реакции замещения при атоме углерода
- 5.1.2.1. Протонный обмен
- 5.1.2.2. Нитрование
- 5.1.2.3. Сульфирование
- 5.1.2.4. Галогенирование
- 5.1.2.5. Ацетоксимеркурирование
- 5.1.2.6. Реакции замещения в пиридинах, содержащих активированный атом азота и кислородсодержащие заместители
- 5.2. Реакции с окислителями
- 5.3. Реакции с нуклеофильными реагентами
- 5.3.1. Нуклеофильное замещение атома водорода
- 5.3.1.1. Алкилирование и арилирование
- 5.3.1.2. Аминирование
- 5.3.1.3. Гидроксилирование
- 5.3.2. Нуклеофильное замещение хорошо уходящих групп
- 5.4. Реакции с основаниями
- 5.4.1. Депротонирование при атоме углерода
- 5.5. Реакции c-металлированных пиридинов
- 5.5.1. Литий- и магнийорганические производные
- 5.5.2. Реакции, катализируемые палладием
- 5.6. Реакции со свободными радикалами, реакции пиридил-радикалов
- 5.6.1. Галогенирование
- 5.6.2. Реакции с углеродными радикалами
- 5.6.3. Димеризация
- 5.6.4. Пиридил-радикалы
- 5.7. Реакции с восстановителями
- 5.8. Электроциклические реакции (основного состояния)
- 5.9. Фотохимические реакции
- 5.10. Окси- и аминопиридины
- 5.10.2. Реакции пиридонов
- 5.10.2.1. Электрофильное присоединение и замещение
- 5.10.2.2. Депротонирование и реакции солей
- 5.10.2.3. Замещение атома кислорода
- 5.10.2.4. Тио-2-пиридоны
- 5.10.3. Реакции аминопиридинов
- 5.10.3.1. Электрофильное присоединение и замещение
- 5.10.3.2. Реакции аминогруппы
- 5.11. Алкилпиридины
- 5.12. Пиридиновые альдегиды, кетоны, карбоновые кислоты и их эфиры
- 5.13. Четвертичные пиридиниевые соли
- 5.13.1. Восстановление и окисление
- 5.13.2. Присоединение металлоорганических реагентов
- 5.13.3. Другие реакции нуклеофильного присоединения
- 5.13.4. Нуклеофильное присоединение с последующим раскрытием цикла
- 5.13.5. Реакции циклизации с участием α-положений или α-заместителей
- 5.13.6. N-Дезалкилирование
- 5.14. N-оксиды пиридина
- 5.14.1. Электрофильное присоединение и замещение
- 5.14.2. Нуклеофильное присоединение и замещение
- 5.14.3. Перегруппировки
- 5.15. Синтез пиридинов
- 5.15.1. Синтез кольца
- 5.15.1.1. Из аммиака и 1,5-дикарбонильных соединений
- 5.15.1.2. Из альдегида, двух молекул 1,3-дикарбонильного соединения и аммиака
- 5.15.1.2.1. Синтез Ганча
- 5.15.1.3. Из 1,3-Дикарбонильных соединений и 3-аминоенонов или 3-аминонитрилов
- 5.15.1.3.1. Синтез Гуарески
- 5.15.1.4. С использованием реакций циклоприсоединения
- 5.15.1.5. С использованием термической электроциклизации
- 5.15.1.6. Из фуранов
- 5.15.1.7. Прочие методы
- 5.15.2. Примеры синтезов некоторых важных производных пиридина
- 5.15.2.1. Фузариновая кислота
- 5.15.2.2. Пиридоксин
- 5.15.2.3. 2-Метокси-4-метил-5-нитропиридин
- 5.15.2.4. Немертеллин
Дополнительно:
В книге изложены важнейшие химические, физико-химические и технологические ...
«Справочник по химии» предназначен для учащихся 7-10 классов. Он содержит сведения ...
 Курс технической химии
Курс технической химии Хозяйственные и технические руководства, издаваемые от императорского вольного ...
 Биографии великих химиков
Биографии великих химиков В книгу, написанную коллективом авторов из ГДР, включены биографические очерки о ...