5.13.1. Восстановление и окисление
Окисление пиридиниевых солей [186] в пиридоны под действием щелочного раствора гексацианоферрита предположительно проходит с участием аддукта пиридиниевого катиона и гидроксид-иона, присутствующего в реакционной смеси в очень малой концентрации. 3-Замещённые пиридиниевые соли превращаются в смесь 2- и 6-пиридонов: так, окисление иодида 1,3-диметилпириди-ния приводит к смеси 2- и 6-пиридонов в соотношении 9:1.
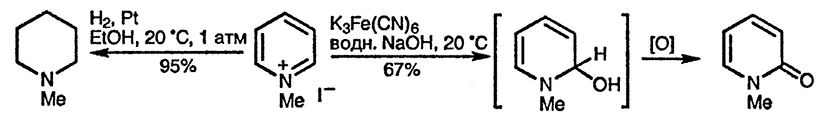
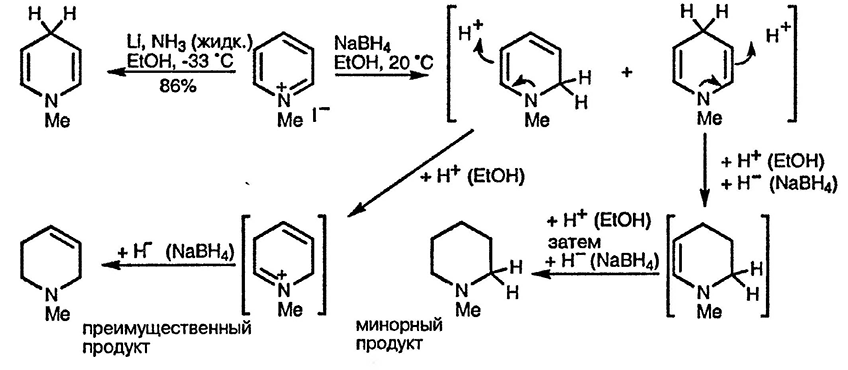
Каталитическое восстановление пиридиниевых солей в пиперидины проходит с исключительной лёгкостью. Пиридиниевые соли подвергаются также гидридному восстановлению при использовании комплексных гидридов металлов [187], формиатов [188] и восстановительной системы литий — жидкий аммиак [189]. При восстановлении боргвдридом натрия в присутствии протонной кислоты преимущественно образуются тетрагидропиридины аллиламинного строения, то есть двойная связь локализована в 3,4-положении. Такой циклический аллиламин образуется в результате присоединения гидрид-иона первоначально по положению 2, протонирования енамина по β-положению и присоединения ещё одного гидрид-иона.
При таком восстановлении всегда образуется некоторое количество полностью восстановленного соединения, и его содержание увеличивается с увеличением объёма заместителя при атоме азота, поскольку это повышает вероятность первоначальной атаки гидрид-ионом по положению 4 с образованием диенамина, способного к двум последовательным процессам протонирования — присоединения гидрид-иона, описанным выше. При восстановлении 3-замещенных пиридиниевых солей образуются β-замещённые 1,2,5,6-тетрагидропиридины. Необходимо соблюдать осторожность при разложении комплекса амин — боран, который может образовываться на заключительном этапе такого восстановления [190]. В смеси 1,4-дигидро-1-метил- и 1,2-дигидро-1-метилпиридинов, приведённой в состояние равновесия под действием сильного основания, соотношение изомеров составляет 9:1 с преобладанием 1,4-дигидропроизводного [191].
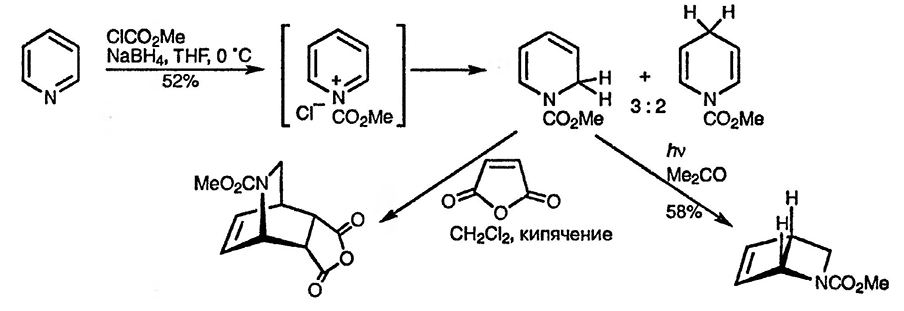
При восстановлении N-ацил- и, в особенности, N-алкокси- или N-арил-оксикарбонилпиридиниевых солей боргидридом зафиксировано образование дигидропроизводных [192], но дальнейшего восстановления не происходит, поскольку образующийся при первоначальном присоединении гидрид-иона енамид в отличие от енамина не может протонироваться в условиях реакции [193].
1,2-Дигидропроизводные, которые получают без примеси 1,4-дигидроизомеров при восстановлении в метаноле при 70 °C, можно использовать в качестве диенов в реакции Дильса-Альдера. При облучении 1,2-дигидропиридин превращается в азабицикло[2.2.0]гексан, который В результате последовательных превращений — удаления карбаматной группы, алкилирования и термической обработки — превращается в нестабильный N-алкилдигидропиридин [194].
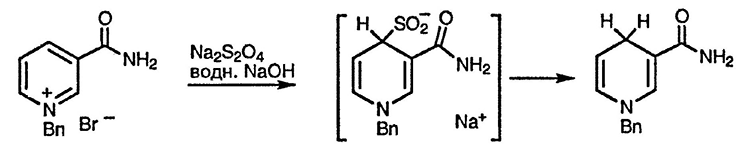
Лёгкое специфическое восстановление 3-ацилпиридиниевых солей дитионитом натрия, приводящее к стабильным 3-ацил-1,4-дигидропиридинам, часто упоминается, поскольку позволяет ощутить значимость коферментной активности никотинамида. На первой стадии такого восстановления происходит присоединение атома серы дитионит-иона по положению 4 [195], как показано ниже. 1,4-Дигидропиридины обычно чувствительны к кислороду воздуха, легко окисляются до соответствующих ароматических структур; стабильность 3-ацил-1,4-дигидропиридинов связана с сопряжением между кольцевым атомом азота и боковой карбонильной группой (см. также синтез Ганча, разд. 5.15.1.2.), Восстановлению дитионитом натрия в соответствующие 1,4-дигидропроизводные могут быть подвергнуты пиридиниевые соли с алкильным заместителем при атоме азота, большим, чем пропил, или, например, с бензильным заместителем [196].
Глава 5
- 5. Пиридины: реакции и методы синтеза
- 5.1. Реакции с электрофильными реагентами
- 5.1.1. Присоединение к атому азота
- 5.1.1.1. Протонирование атома азота
- 5.1.1.2. Нитрование по атому азота
- 5.1.1.3. Аминирование по атому азота
- 5.1.1.4. Окисление атома азота
- 5.1.1.5. Сульфирование по атому азота
- 5.1.1.6. Галогенирование по атому азота
- 5.1.1.7. Ацилирование по атому азота
- 5.1.1.8. Алкилирование по атому азота
- 5.1.1.9. Реакции комплексообразования
- 5.1.2. Реакции замещения при атоме углерода
- 5.1.2.1. Протонный обмен
- 5.1.2.2. Нитрование
- 5.1.2.3. Сульфирование
- 5.1.2.4. Галогенирование
- 5.1.2.5. Ацетоксимеркурирование
- 5.1.2.6. Реакции замещения в пиридинах, содержащих активированный атом азота и кислородсодержащие заместители
- 5.2. Реакции с окислителями
- 5.3. Реакции с нуклеофильными реагентами
- 5.3.1. Нуклеофильное замещение атома водорода
- 5.3.1.1. Алкилирование и арилирование
- 5.3.1.2. Аминирование
- 5.3.1.3. Гидроксилирование
- 5.3.2. Нуклеофильное замещение хорошо уходящих групп
- 5.4. Реакции с основаниями
- 5.4.1. Депротонирование при атоме углерода
- 5.5. Реакции c-металлированных пиридинов
- 5.5.1. Литий- и магнийорганические производные
- 5.5.2. Реакции, катализируемые палладием
- 5.6. Реакции со свободными радикалами, реакции пиридил-радикалов
- 5.6.1. Галогенирование
- 5.6.2. Реакции с углеродными радикалами
- 5.6.3. Димеризация
- 5.6.4. Пиридил-радикалы
- 5.7. Реакции с восстановителями
- 5.8. Электроциклические реакции (основного состояния)
- 5.9. Фотохимические реакции
- 5.10. Окси- и аминопиридины
- 5.10.2. Реакции пиридонов
- 5.10.2.1. Электрофильное присоединение и замещение
- 5.10.2.2. Депротонирование и реакции солей
- 5.10.2.3. Замещение атома кислорода
- 5.10.2.4. Тио-2-пиридоны
- 5.10.3. Реакции аминопиридинов
- 5.10.3.1. Электрофильное присоединение и замещение
- 5.10.3.2. Реакции аминогруппы
- 5.11. Алкилпиридины
- 5.12. Пиридиновые альдегиды, кетоны, карбоновые кислоты и их эфиры
- 5.13. Четвертичные пиридиниевые соли
- 5.13.1. Восстановление и окисление
- 5.13.2. Присоединение металлоорганических реагентов
- 5.13.3. Другие реакции нуклеофильного присоединения
- 5.13.4. Нуклеофильное присоединение с последующим раскрытием цикла
- 5.13.5. Реакции циклизации с участием α-положений или α-заместителей
- 5.13.6. N-Дезалкилирование
- 5.14. N-оксиды пиридина
- 5.14.1. Электрофильное присоединение и замещение
- 5.14.2. Нуклеофильное присоединение и замещение
- 5.14.3. Перегруппировки
- 5.15. Синтез пиридинов
- 5.15.1. Синтез кольца
- 5.15.1.1. Из аммиака и 1,5-дикарбонильных соединений
- 5.15.1.2. Из альдегида, двух молекул 1,3-дикарбонильного соединения и аммиака
- 5.15.1.2.1. Синтез Ганча
- 5.15.1.3. Из 1,3-Дикарбонильных соединений и 3-аминоенонов или 3-аминонитрилов
- 5.15.1.3.1. Синтез Гуарески
- 5.15.1.4. С использованием реакций циклоприсоединения
- 5.15.1.5. С использованием термической электроциклизации
- 5.15.1.6. Из фуранов
- 5.15.1.7. Прочие методы
- 5.15.2. Примеры синтезов некоторых важных производных пиридина
- 5.15.2.1. Фузариновая кислота
- 5.15.2.2. Пиридоксин
- 5.15.2.3. 2-Метокси-4-метил-5-нитропиридин
- 5.15.2.4. Немертеллин
Дополнительно:
 Химия синтетических смол (комплект из 4 книг)
Химия синтетических смол (комплект из 4 книг) Книга Эллиса является в настоящее время наиболее полной монографией по химии ...
Монография посвящена математическому моделированию и исследованию нелинейных ...
В справочник включены сведения об органических стабилизаторах, ускорителях и ...
 Комплексы 4d-платиновых металлов с фосфор(III)- и мышьяк(III)- органическими лигандами
Комплексы 4d-платиновых металлов с фосфор(III)- и мышьяк(III)- органическими лигандами В монографии проанализированы и обобщены данные по условиям стабилизации ...