5.11. Алкилпиридины
Главная особенность химических свойств алкилпиридинов состоит в способности алкильных групп, непосредственно связанных с пиридиновым циклом, депротонироваться [167]. Скорости протонного обмена в системе метанол — метилат натрия для 4-, 2- и 3-алкилпиридинов равны соответственно 1800, 130, 1 [168].
Сравнение значений pKa, измеренных в тетрагидрофуране [169], демонстрирует, что γ-изомеры обладают в большей степени кислотными свойствами, чем α-алкилпиридины, а α- и γ-изомеры более сильные кислоты, чем β-изомеры, однако образование того или иного аниона при возможности нескольких конкурирующих процессов депротонирования существенно зависит от ряда условий. Депротонирование при действии алкиллитиевых соединений приводит к образованию α-анионов, более стабильные α-анионы образуются при использовании амидных оснований [170]. Гораздо большая склонность [171] α- и γ-алкил-пиридинов к депротонированию связана с мезомерной стабилизацией соответствующих анионов с участием кольцевого атома азота, что невозможно в случае β-изомера. В последнем случае депротонированию способствует лишь индуктивное влияние кольцевого атома азота, однако при подходящих условиях депротонирование β-метильной группы все же возможно [172]. Различие в реакционной способности метальных групп в положениях 2 и 3 позволяет селективно провести превращения по первой метальной группе [173].
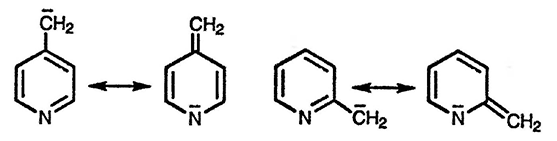
Образующиеся при депротонировании α- и γ- алкильных групп анионы способны принимать участие в различных реакциях [174] и по своим свойствам они аналогичны енолят-анионам. Аналогичное образование анионов наблюдается при депротонировании метальных групп в орто- и пара-толуолах. Металлирование боковой цепи 2-трет-бутилкарбониламино-4-метилпиридина проходит при комнатной температуре [175].
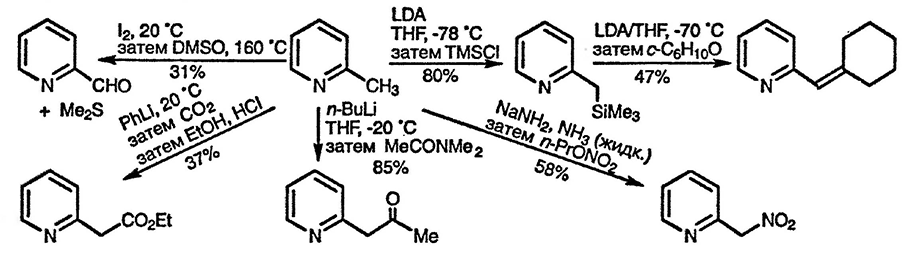
Подвижность атомов водорода боковых алкильных групп четвертичных алкилпиридиниевых солей существенно выше, и реакции конденсации с участием продуктов депротонирования, аналогичных енаминам, проходят в значительно более мягких условиях [176]. Депротонирование боковых алкильных групп возможно и для N-оксидов пиридинов, однако в этом случае такое депротонирование может конкурировать с депротонированием по положению 2 пиридинового цикла [177].
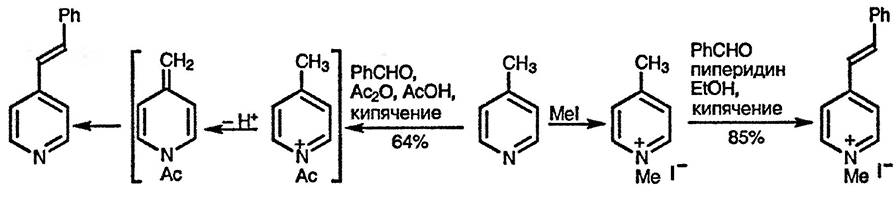
Возможность стабилизации пиридиновым циклом экзоциклического карбанионного центра в α- и γ-положениях проявляется также в способности винил-пиридинов [178] и пиридилацетиленов присоединять нуклеофильные реагенты по типу реакции Михаэля (катализируемая солями ртути гидратация проходит противоположным образом [179]). Кроме того, известно, что 2-(пиридин-2-ил)-и 2-(пиридин-4-ил)этиловые эфиры, сульфиды или сульфоны могут служить защитными группами, легко удаляемыми при алкилировании пиридинового азота метилиодидом, приводящем к элиминированию винилпиридиниевой соли [180].
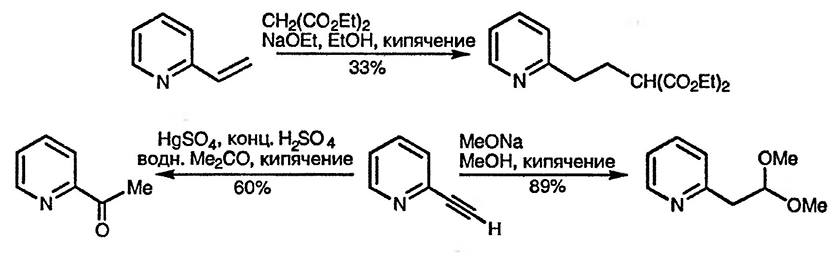
При рассмотрении реакционной способности галогеналкилпиридинов следует учитывать, что расчётные данные, а также масс-спектральные измерения свидетельствуют о существенной стабильности α-пиридилалкильных катионов вследствие взаимодействия катионного центра с копланарной неподелённой электронной парой атома азота [181].
Глава 5
- 5. Пиридины: реакции и методы синтеза
- 5.1. Реакции с электрофильными реагентами
- 5.1.1. Присоединение к атому азота
- 5.1.1.1. Протонирование атома азота
- 5.1.1.2. Нитрование по атому азота
- 5.1.1.3. Аминирование по атому азота
- 5.1.1.4. Окисление атома азота
- 5.1.1.5. Сульфирование по атому азота
- 5.1.1.6. Галогенирование по атому азота
- 5.1.1.7. Ацилирование по атому азота
- 5.1.1.8. Алкилирование по атому азота
- 5.1.1.9. Реакции комплексообразования
- 5.1.2. Реакции замещения при атоме углерода
- 5.1.2.1. Протонный обмен
- 5.1.2.2. Нитрование
- 5.1.2.3. Сульфирование
- 5.1.2.4. Галогенирование
- 5.1.2.5. Ацетоксимеркурирование
- 5.1.2.6. Реакции замещения в пиридинах, содержащих активированный атом азота и кислородсодержащие заместители
- 5.2. Реакции с окислителями
- 5.3. Реакции с нуклеофильными реагентами
- 5.3.1. Нуклеофильное замещение атома водорода
- 5.3.1.1. Алкилирование и арилирование
- 5.3.1.2. Аминирование
- 5.3.1.3. Гидроксилирование
- 5.3.2. Нуклеофильное замещение хорошо уходящих групп
- 5.4. Реакции с основаниями
- 5.4.1. Депротонирование при атоме углерода
- 5.5. Реакции c-металлированных пиридинов
- 5.5.1. Литий- и магнийорганические производные
- 5.5.2. Реакции, катализируемые палладием
- 5.6. Реакции со свободными радикалами, реакции пиридил-радикалов
- 5.6.1. Галогенирование
- 5.6.2. Реакции с углеродными радикалами
- 5.6.3. Димеризация
- 5.6.4. Пиридил-радикалы
- 5.7. Реакции с восстановителями
- 5.8. Электроциклические реакции (основного состояния)
- 5.9. Фотохимические реакции
- 5.10. Окси- и аминопиридины
- 5.10.2. Реакции пиридонов
- 5.10.2.1. Электрофильное присоединение и замещение
- 5.10.2.2. Депротонирование и реакции солей
- 5.10.2.3. Замещение атома кислорода
- 5.10.2.4. Тио-2-пиридоны
- 5.10.3. Реакции аминопиридинов
- 5.10.3.1. Электрофильное присоединение и замещение
- 5.10.3.2. Реакции аминогруппы
- 5.11. Алкилпиридины
- 5.12. Пиридиновые альдегиды, кетоны, карбоновые кислоты и их эфиры
- 5.13. Четвертичные пиридиниевые соли
- 5.13.1. Восстановление и окисление
- 5.13.2. Присоединение металлоорганических реагентов
- 5.13.3. Другие реакции нуклеофильного присоединения
- 5.13.4. Нуклеофильное присоединение с последующим раскрытием цикла
- 5.13.5. Реакции циклизации с участием α-положений или α-заместителей
- 5.13.6. N-Дезалкилирование
- 5.14. N-оксиды пиридина
- 5.14.1. Электрофильное присоединение и замещение
- 5.14.2. Нуклеофильное присоединение и замещение
- 5.14.3. Перегруппировки
- 5.15. Синтез пиридинов
- 5.15.1. Синтез кольца
- 5.15.1.1. Из аммиака и 1,5-дикарбонильных соединений
- 5.15.1.2. Из альдегида, двух молекул 1,3-дикарбонильного соединения и аммиака
- 5.15.1.2.1. Синтез Ганча
- 5.15.1.3. Из 1,3-Дикарбонильных соединений и 3-аминоенонов или 3-аминонитрилов
- 5.15.1.3.1. Синтез Гуарески
- 5.15.1.4. С использованием реакций циклоприсоединения
- 5.15.1.5. С использованием термической электроциклизации
- 5.15.1.6. Из фуранов
- 5.15.1.7. Прочие методы
- 5.15.2. Примеры синтезов некоторых важных производных пиридина
- 5.15.2.1. Фузариновая кислота
- 5.15.2.2. Пиридоксин
- 5.15.2.3. 2-Метокси-4-метил-5-нитропиридин
- 5.15.2.4. Немертеллин
Дополнительно:
Синтез полимеров методом поликонденсации представляет значительный интерес при ...
 Структура и прочность полимеров
Структура и прочность полимеров В книге собраны и систематизированы результаты работ советских и зарубежных ...
 Поливинилхлорид в промышленности
Поливинилхлорид в промышленности Книга инженеров X. Юнгникеля и X. Виппенхона «Поливинилхлорид в промышленности» ...