5.15.1.3.1. Синтез Гуарески
Использование цианацетамида в качестве азотсодержащего соединения в конденсации с 1,3-дикарбонильными соединениями приводит к образованию 3-циано-2-пиридона, карбонильная и циано-группы которого могут быть впоследствии удалены.
При введении в реакцию с 3-аминоеноном, аминоакрилатом и цианацетамидом дикарбонильного соединения, карбонильные группы которого существенно различаются по реакционной способности, можно получить только один из двух возможных изомерных пиридинов или пиридонов в результате реакции с участием наиболее электрофильного карбонильного атома углерода [264] [265].
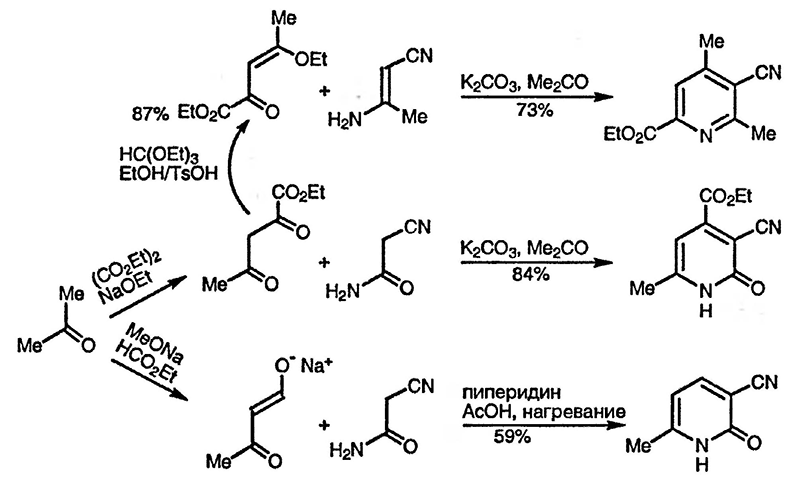
При использовании ацетиленовых кетонов региоселективность реакции контролируется сопряжённым присоединением цианацетамида [266]; аналогично в случае 3-алкоксиенонов (то есть эфиров енолов 1,3-дикетонов) протекающая на первой стадии реакция Михаэля определяет региоселективность синтеза производных пиридина [264] [267]. Применение H2NCOCH2C(NH2) = N + H2Cl- вместо цианацетамида позволяет получать амиды 2-аминопиридин-3-карбоновых кислот [268], в то время как использование H2NCOCH2NO2 вместо цианацетамида приводит к 3-нитро-2-пиридонам [269].
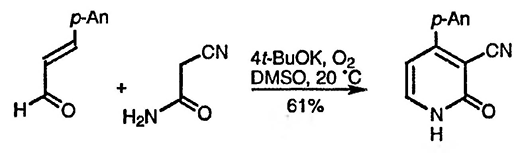
Успешное образование пиридинового цикла возможно также при использовании исходных соединений в более низкой степени окисления: дегидрирование может быть осуществлено либо кислородом воздуха, либо привнесённым в реакционную смесь кислородом (например, возможно использование вместо 1,3-дикарбонильного соединения α,β-ненасыщенных кетонов и альдегидов, как показано ниже) [270]:
Глава 5
- 5. Пиридины: реакции и методы синтеза
- 5.1. Реакции с электрофильными реагентами
- 5.1.1. Присоединение к атому азота
- 5.1.1.1. Протонирование атома азота
- 5.1.1.2. Нитрование по атому азота
- 5.1.1.3. Аминирование по атому азота
- 5.1.1.4. Окисление атома азота
- 5.1.1.5. Сульфирование по атому азота
- 5.1.1.6. Галогенирование по атому азота
- 5.1.1.7. Ацилирование по атому азота
- 5.1.1.8. Алкилирование по атому азота
- 5.1.1.9. Реакции комплексообразования
- 5.1.2. Реакции замещения при атоме углерода
- 5.1.2.1. Протонный обмен
- 5.1.2.2. Нитрование
- 5.1.2.3. Сульфирование
- 5.1.2.4. Галогенирование
- 5.1.2.5. Ацетоксимеркурирование
- 5.1.2.6. Реакции замещения в пиридинах, содержащих активированный атом азота и кислородсодержащие заместители
- 5.2. Реакции с окислителями
- 5.3. Реакции с нуклеофильными реагентами
- 5.3.1. Нуклеофильное замещение атома водорода
- 5.3.1.1. Алкилирование и арилирование
- 5.3.1.2. Аминирование
- 5.3.1.3. Гидроксилирование
- 5.3.2. Нуклеофильное замещение хорошо уходящих групп
- 5.4. Реакции с основаниями
- 5.4.1. Депротонирование при атоме углерода
- 5.5. Реакции c-металлированных пиридинов
- 5.5.1. Литий- и магнийорганические производные
- 5.5.2. Реакции, катализируемые палладием
- 5.6. Реакции со свободными радикалами, реакции пиридил-радикалов
- 5.6.1. Галогенирование
- 5.6.2. Реакции с углеродными радикалами
- 5.6.3. Димеризация
- 5.6.4. Пиридил-радикалы
- 5.7. Реакции с восстановителями
- 5.8. Электроциклические реакции (основного состояния)
- 5.9. Фотохимические реакции
- 5.10. Окси- и аминопиридины
- 5.10.2. Реакции пиридонов
- 5.10.2.1. Электрофильное присоединение и замещение
- 5.10.2.2. Депротонирование и реакции солей
- 5.10.2.3. Замещение атома кислорода
- 5.10.2.4. Тио-2-пиридоны
- 5.10.3. Реакции аминопиридинов
- 5.10.3.1. Электрофильное присоединение и замещение
- 5.10.3.2. Реакции аминогруппы
- 5.11. Алкилпиридины
- 5.12. Пиридиновые альдегиды, кетоны, карбоновые кислоты и их эфиры
- 5.13. Четвертичные пиридиниевые соли
- 5.13.1. Восстановление и окисление
- 5.13.2. Присоединение металлоорганических реагентов
- 5.13.3. Другие реакции нуклеофильного присоединения
- 5.13.4. Нуклеофильное присоединение с последующим раскрытием цикла
- 5.13.5. Реакции циклизации с участием α-положений или α-заместителей
- 5.13.6. N-Дезалкилирование
- 5.14. N-оксиды пиридина
- 5.14.1. Электрофильное присоединение и замещение
- 5.14.2. Нуклеофильное присоединение и замещение
- 5.14.3. Перегруппировки
- 5.15. Синтез пиридинов
- 5.15.1. Синтез кольца
- 5.15.1.1. Из аммиака и 1,5-дикарбонильных соединений
- 5.15.1.2. Из альдегида, двух молекул 1,3-дикарбонильного соединения и аммиака
- 5.15.1.2.1. Синтез Ганча
- 5.15.1.3. Из 1,3-Дикарбонильных соединений и 3-аминоенонов или 3-аминонитрилов
- 5.15.1.3.1. Синтез Гуарески
- 5.15.1.4. С использованием реакций циклоприсоединения
- 5.15.1.5. С использованием термической электроциклизации
- 5.15.1.6. Из фуранов
- 5.15.1.7. Прочие методы
- 5.15.2. Примеры синтезов некоторых важных производных пиридина
- 5.15.2.1. Фузариновая кислота
- 5.15.2.2. Пиридоксин
- 5.15.2.3. 2-Метокси-4-метил-5-нитропиридин
- 5.15.2.4. Немертеллин
Дополнительно:
 Основные процессы переработки полимеров (теория и методы расчёта)
Основные процессы переработки полимеров (теория и методы расчёта) В книге систематизированы современные представления в области реологии ...
В книге даётся богатейший, хорошо систематизированный справочный материал по ...
