Глава 17. Упражнения повышенной сложности
1. Индол вступает в реакцию со смесью N-метил-2-пиперидона и POCl3 с последующей обработкой NaOH, давая соединение с брутто-формулой C14H18N2O. Каково его строение?
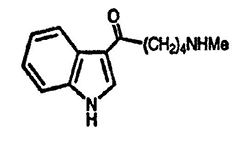
2. Предложите структуру тетрациклического соединения с брутто-формулой C18H19NO, образующегося при обработке 3-метилиндола 2-гидрокси-3,5-диметилбензилхлоридом.
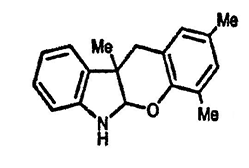
3. Если индольный димер (разд. 17.1.9) подвергнуть кислотной обработке в присутствии индола, образуется «тример индола» — C24H21N3. Предложите структуру этого «тримера» (подсказка: рассмотрите, какой из двух реагентов легче протонируется и по какому атому).
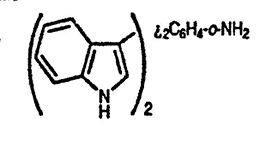
4. Как, исходя из индола и используя общий интермедиат, можно получить следующие соединения:
а) 3-индолилуксусную кислоту и
б) триптамин?
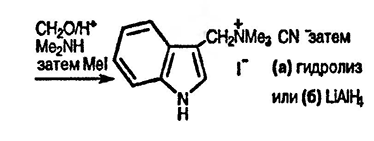
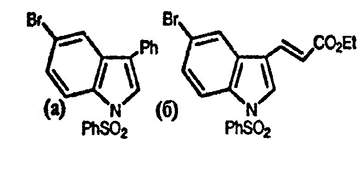
5. Что образуется при взаимодействии 5-бром-3-иод-1-фенилсульфонилиндола
а) с PhB(OH)2/Pd(PPh3)4/водн. Na2CO3 и
б) с этилакрилатом/Pd(OAc)2/Ph3P/Et3N?
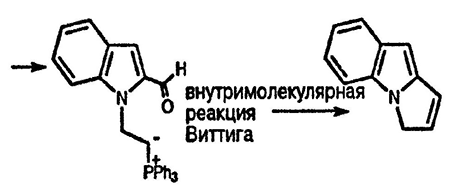
6. Предложите механизм реакции и структуру образующегося из 2-формилиндола трициклического соединения с брутто-формулой C11H9N при обработке NaH и Ph3P+CH=CH2Br-.
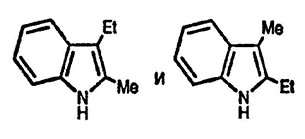
7. При обработке 3-этил-3-метил-3Н-индола кислотой образуются два продукта, каждый из которых изомерен исходному соединению. Предложите структуры и объясните образование этих двух соединений.
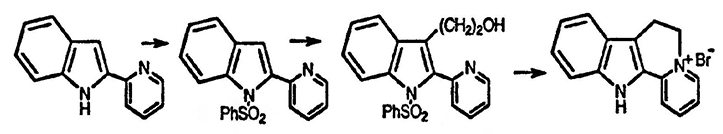
8. Предложите структуру соли C15H13N2+Br-, образующейся в следующей последовательности превращений: 2-(2-пиридил)индол реагирует сначала с н-BuLi, затем с PhSO2Cl → C14H10INO2S, затем это соединение последовательно взаимодействуете трет-BuLi при −100 °C, а затем с этиленоксидом (→ C21H18N2O3S), водн. NaOH (→ C15H14N2O) и, наконец, с PBr3.
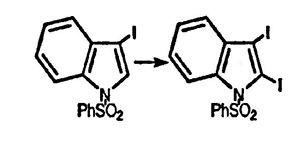
9. Какие соединения образуются в следующей последовательности взаимодействий: индол/н-BuLi, затем I2, затем PhSO2Cl → C14H10INO2S, затем это соединение реагирует с диизопропиламидом лития, затем с I2 → C14H9I2NO2S?
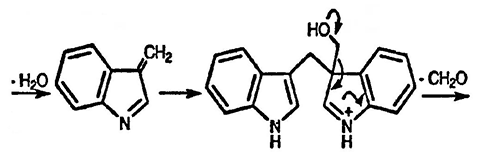
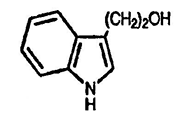
10. При нагревании индол-3-ил-CH2OH с кислотой образуется ди(индол-3-ил)метан. Каков механизм этого превращения?
11. Каково строение соединения с брутто-формулой C10H11NO), образующегося при кипячении смеси фенилгидразина и 2,3-дигидрофурана в уксусной кислоте?
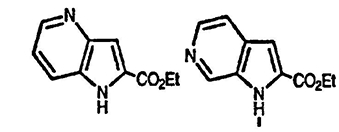
12. Нарисуйте структуры азаиндолов, образующихся при обработке 2-метил-3-нитро- и 4-метил-3-нитропиридинов соответственно (EtO2C)2/EtONa, а затем H2/Pd-C. Оба соединения имеют одинаковые брутто-формулы C10H10N2O2.
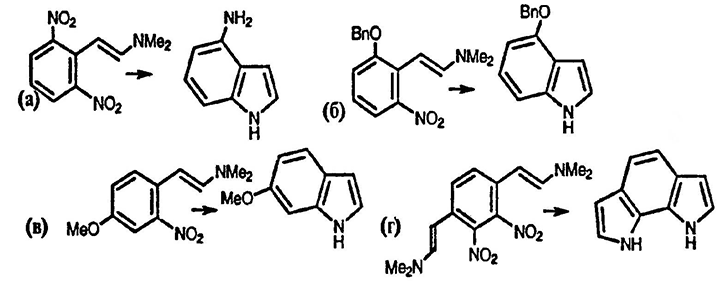
13. Нагревание диметилацеталя диметилформамида с перечисленными ниже ароматическими соединениями приводит к образованию продуктов конденсации, а последующее взаимодействие с указанным реагентом даёт индолы. Нарисуйте структуры соединений — продуктов конденсации и индолов:
а) 2,6-динитротолуол, затем TiCl3 → C8H8N2;
б) 2-бензилокси-6-нитротолуол, затем H2/Pt → C15H13NO;
в) 4-метокси-2-нитротолуол, затем H2/Pd → C9H9NO;
г) 2,3-динитро-1,4-диметилбензол, затем H2/Pd → C10H8N2.
Глава 17
- 17. Индолы: реакции и методы синтеза
- 17.1. Реакции с электрофильными реагентами
- 17.1.1. Протонирование
- 17.1.2. Нитрование; реакции с другими азотсодержащими электрофилами
- 17.1.3. Сульфирование; реакции с другими серосодержащими электрофилами
- 17.1.4. Галогенирование
- 17.1.5. Ацилирование
- 17.1.6. Алкилирование
- 17.1.7. Реакции с альдегидами и кетонами
- 17.1.8. Реакции с α,β-ненасыщенными кетонами, нитрилами и нитросоединениями
- 17.1.9. Реакции с иминиевыми ионами: реакция Манниха
- 17.1.10. Диазосочетание и нитрозирование
- 17.1.11. Электрофильное металлирование
- 17.1.11.1. Меркурирование
- 17.1.11.2. Таллирование
- 17.1.11.3. Палладирование
- 17.2. Реакции с окислителями
- 17.3. Реакции с нуклеофильными реагентами
- 17.4. Реакции с основаниями
- 17.4.1. Депротонирование N-водорода
- 17.4.2. Депротонирование C-водорода
- 17.5. Реакции N-металлированных индолов
- 17.6. Реакции C-металлированных индолов
- 17.6.1. Литийорганические производные
- 17.6.2. Реакции, катализируемые палладием
- 17.7. Реакции со свободными радикалами
- 17.8. Реакции с восстановителями
- 17.9. Реакции с карбенами
- 17.10. Электроциклические и фотохимические реакции
- 17.11. Алкилиндолы
- 17.12. Реакции C-замещённых индольных соединений
- 17.13. Индолкарбоновые кислоты
- 17.14. Гидроксииндолы
- 17.14.1. Оксиндол
- 17.14.2. Индоксил
- 17.14.3. Изатин
- 17.14.4. 1-Гидроксиндол
- 17.15. Аминоиндолы
- 17.16. Азаиндолы
- 17.16.1. Реакции электрофильного замещения
- 17.16.2. Реакции нуклеофильного замещения
- 17.17. Синтезы индолов
- 17.17.1. Синтезы кольца
- 17.17.1.1. Из фенилгидразонов альдегидов и кетонов
- 17.17.1.2. Из o-(2-оксоалкил)анилинов
- 17.17.1.3. Из o-алкинилариламинов
- 17.17.1.4. Из o-толуидинов
- 17.17.1.5. Из α-ариламинокарбонильных соединений
- 17.17.1.6. Синтез из пирролов
- 17.17.1.7. Из орто-замещённых нитроаренов
- 17.17.1.8. Из N-ариленаминов
- 17.17.1.9. Из N-аллил-o-галогенариламинов
- 17.17.1.10. Из енаминов и п-хинонов
- 17.17.1.11. Из ариламинов
- 17.17.1.12. Из o-ациланилидов
- 17.17.1.13. Из o-изоцианостиролов
- 17.17.1.14. Из o-хлорацетилариламинов
- 17.17.1.15. Циклизацией нитренов
- 17.17.1.16. Циклизации аринов
- 17.17.1.17. Из o-нитростиролов
- 17.17.1.18. Из индолинов
- 17.17.2. Синтезы оксиндолов
- 17.17.3. Синтезы индоксилов
- 17.17.4. Синтез изатинов
- 17.17.5. Синтезы 1-гидроксиндолов
- 17.17.6. Примеры синтезов некоторых важных производных индола
- 17.17.6.1. Ондансетрон
- 17.17.6.2. Стауроспорин агликон
- 17.17.6.3. Серотонин
- 17.17.6.4. Хуангксинмицин
- 17.17.7. Синтезы азаиндолов
Дополнительно:
Ленинград, 1959 год. Государственное научно-техническое издательство химической ...
В сборник включены наиболее интересные статьи по теории и практике переработки ...
 Химия и технология полимерных плёнок
Химия и технология полимерных плёнок Книга посвящена химии и технологии производства плёночных материалов из ...
