13.18.1.2. Из α-аминокарбонильных соединений и активированных кетонов
α-Аминокетоны взаимодействуют с карбонильными соединениями, обладающими α-метиленовой группой, преимущественно активированной дополнительным акцепторным заместителем, как, например, в эфирах β-кетокислот
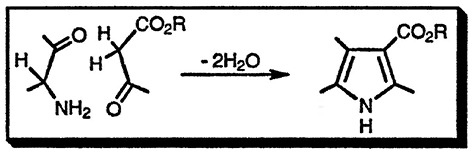
Синтез Кнорра
Широко используемый общий подход к синтезу производных пиррола связан с использованием двух компонентов: один — α-аминокарбонильное соединение, которое поставляет в будущий пиррольный цикл атом азота и атомы углерода C(2) и C(3), и второй компонент, поставляющий атомы C(4) и C(5), в котором должна быть метальная группа в α-положении к карбонильной. Синтез Кнорра эффективен только в том случае, если метиленовая группа дополнительно активирована (например, как в ацетоуксусном эфире); при этом конденсация, приводящая к пирролу, успешно конкурирует с самоконденсацией α-аминокарбонильных соединений. Ниже в качестве иллюстрации приведён синтез 4-метилпиррол-3-карбоновой кислоты и её последующее превращение в 3-метилпиррол:
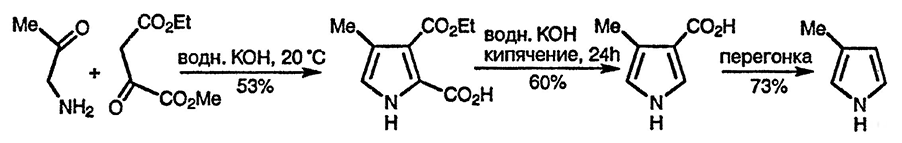
Поскольку α-аминокарбонильные соединения очень легко претерпевают самоконденсацию с образованием дигидропиразинов (разд. 11.13.), их обычно получают и используют в виде солей с высвобождением соответствующих свободных оснований под действием оснований, присутствующих в реакционной смеси. Альтернативно в синтезе Кнорра используются аминокарбонильные соединения с защищённой карбонильной группой, такие, как аминоацеталь [H2NCH2CH(OEt)2], вместе с эфирами енолов 1,3-дикетонов в качестве предшественников активированных карбонильных соединений [143]
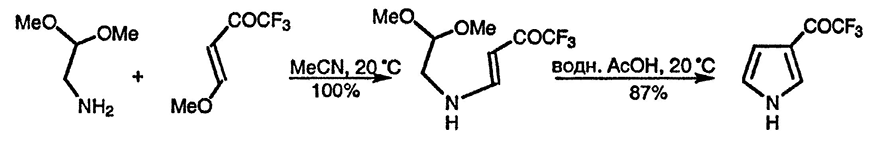
Избежать прямого использования α-аминокарбонильных соединений можно, получая их в присутствии второго компонента синтеза Кнорра. В качестве восстановителя для превращения оксиминной группы в аминную, применяют цинк в уксусной кислоте и дитионит натрия [144]; при этом кетонная и сложноэфирная группы остаются незатронутыми
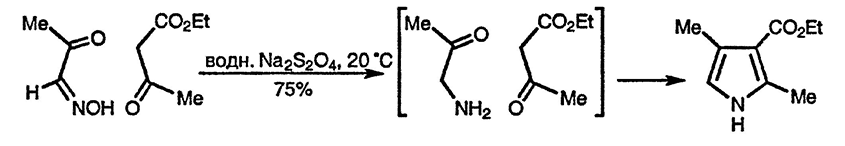
В классическом варианте синтеза Кнорра в качестве α-аминокарбонильной компоненты используется аминопроизводное другой карбонильной компоненты, которое генерируется из оксиминопроизводного in situ [145]
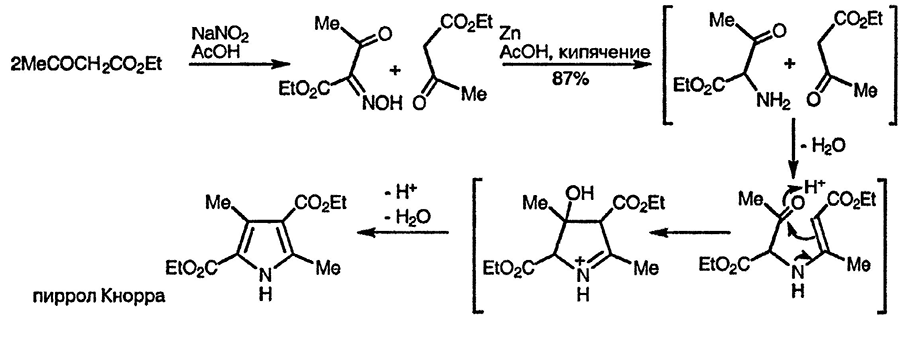
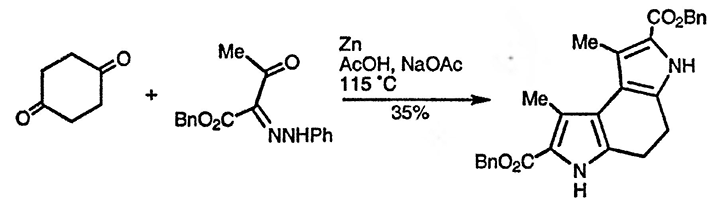
Согласно предполагаемому механизму процесса, показанному на примере образования пиррола Кнорра, на первой стадии происходит образование связи N — C(2), что предполагает присоединение атома азота к более электрофильной из двух карбонильных групп второй компоненты. Аналогично образование связи C(3) — C(4) происходит с участием более электрофильной (когда возможно альтернативное течение реакции) карбонильной группы α-аминокарбонильной компоненты. Существует множество элегантных примеров применения этого подхода к синтезу производных пиррола. Интересен пример образования двух пиррольных циклов при использовании в качестве предшественника α-амино-карбонильного соединения фенилгидразона, как показано ниже [146]:
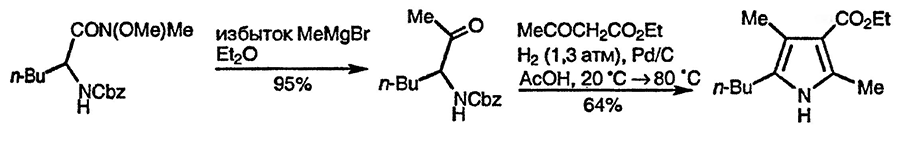
Современные подходы к α-аминокарбонильным соединениям основаны на реакции 2-бромкетонов с диформамидом натрия с образованием α-формамидо-кетонов [147] и на взаимодействии амидов Вайнреба N-защищённых α-аминокислот с реактивами Гриньяра с последующим удалением N-защитной группы в присутствии второго компонента, как показано ниже [148]. Гидридное восстановление амидов Вайнреба N-защищённых α-аминокислот приводит к образованию α-аминоальдегидов, также используемых в этом подходе к синтезу производных пиррола [149].
Бис(метилтио)нитроэтилен при взаимодействии с органическими купратами замещает одну метилтиогруппу на алкильную или арильную. Далее продукт этой реакции при взаимодействии с аминоацеталями, (в качестве предшественников α-аминокарбонильных соединений) превращается в ациклическое соединение, замыкание цикла в котором приводит к 2-замещённым 3-нитро-пирролам [150].
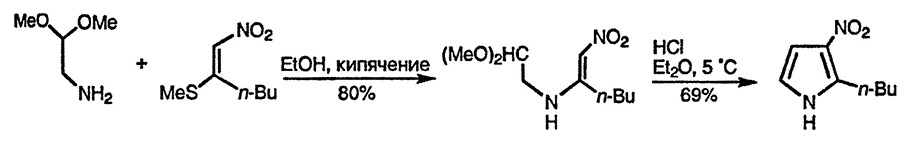
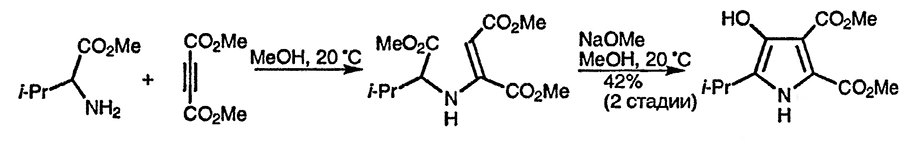
Енамины, образующиеся при присоединении эфиров α-аминокислот к диметиловому эфиру ацетилен-дикарбоновой кислоты, способны превращаться в 3-гидроксипирролы в результате замыкания цикла по типу конденсации Кляйзена [151].
13.18.1.2. Из α-аминокарбонильных соединений и активированных кетонов
Список литературы к главе 13
Упражнения к главе 13
Глава 13
- 13. Пирролы: реакции и методы синтеза
- 13.1. Реакции с электрофильными реагентами
- 13.1.1. Протонирование
- 13.1.1.1. Реакции протонированных пирролов
- 13.1.2. Нитрование
- 13.1.3. Сульфирование и реакции с использованием других серосодержащих электрофильных реагентов
- 13.1.4. Галогенирование
- 13.1.5. Ацилирование
- 13.1.6. Алкилирование
- 13.1.7. Конденсация с альдегидами и кетонами
- 13.1.8. Конденсации с иминами и иминиевыми ионами
- 13.1.9. Сочетание с солями диазония
- 13.2. Реакции с окислителями
- 13.3. Реакции с нуклеофильными реагентами
- 13.4. Реакции с основаниями
- 13.4.1. Депротонирование атома азота
- 13.4.2. Депротонирование по атому углерода
- 13.5. Реакции N-металлированных производных пиррола
- 13.5.1. Литий-, натрий-, калий-, магний- и цинкорганические производные
- 13.6. Реакции C-металлированных производных пиррола
- 13.6.1. Литийорганические производные
- 13.6.2. Реакции, катализируемые палладием
- 13.7. Реакции с радикальными реагентами
- 13.8. Реакции с восстановителями
- 13.9. Электроциклические реакции (основного состояния)
- 13.10. Реакции с карбенами и карбеноидами
- 13.11. Фотохимические реакции
- 13.12. Реакции пиррил-C-X-соединений
- 13.13. Пирролальдегиды и пирролкетоны
- 13.14. Пирролкарбоновые кислоты
- 13.15. Эфиры пирролкарбоновых кислот
- 13.16. Галогенопирролы
- 13.17. Окси- и аминопирролы
- 13.17.1. 2-Оксипирролы
- 13.17.2. 3-Оксипирролы
- 13.17.3. Аминопирролы
- 13.18. Методы синтеза пирролов
- 13.18.1. Синтез кольца
- 13.18.1.1. Из 1,4-дикарбонильных соединений и аммиака или первичных аминов
- 13.18.1.2. Из α-аминокарбонильных соединений и активированных кетонов
- 13.18.1.3. Из α-галогенокарбонильных соединений
- 13.18.1.4. Из тозилметилизоцианида и α,β-непредельных эфиров или кетонов и из изоцианоацетатов и α,β-непредельных нитросоединений
- 13.18.1.5. Из 1,3-дикарбонильных соединений и эфиров глицина
- 13.18.1.6. Из алкинов и оксидооксазолиевых солей
- 13.18.2.1. Некоторые современные общие подходы к синтезу пиррола
- 13.18.2.2. Из альдегидов, аминов и нитроалканов
- 13.18.2.3. Из 4-аминоацетиленов и из 4-аминоацетиленовых кетонов
- 13.18.2.4. Из 2-аминокетонов через промежуточное образование алкилиденкарбенов
- 13.18.3. Примеры синтезов некоторых важных производных пиррола
- 13.18.3.1. Порфобилиноген
- 13.18.3.2. Октаэтилпорфирин
- 13.18.3.3. Октаэтилпорфирин
- 13.18.3.4. Октаэтилгемипорфицен
- 13.18.3.5. Бензо[1,2-b:4,3-b’]дипиррол
- 13.18.3.6. Эпибатидин
Дополнительно:
 Общая химия. Состояние веществ и химические реакции
Общая химия. Состояние веществ и химические реакции Рассматриваются многообразные химические реакции, систематизированные по ...
 Адольф Кетлэ. Его жизнь и научная деятельность
Адольф Кетлэ. Его жизнь и научная деятельность Воспроизведено в оригинальной авторской орфографии издания 1894 года ...
 Химия свободных радикалов
Химия свободных радикалов Книга Уотерса представляет интерес, поскольку в ней собран обширный материал, ...
 Основные законы химии (комплект из 2 книг)
Основные законы химии (комплект из 2 книг) Учебное пособие к изучению основных законов и представлений общей химии. Автор — ...