13.18.1.1. Из 1,4-дикарбонильных соединений и аммиака или первичных аминов
1,4-Дикарбонильные соединения реагируют с аммиаком или первичными аминами с образованием пирролов [7] [131] [132]
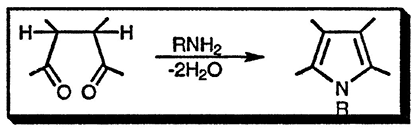
Синтез Пааля-Кнорра
Пирролы образуются при реакции аммиака или первичных аминов с 1,4-дикарбонильными соединениями [132] [134] (см. также разд. 15.13.1.1.). Для синтеза N-незамещённых пирролов вместо аммиака можно использовать гексаметилдисилазид с оксидом алюминия [135]. Образование пиррольного цикла происходит в результате последовательно реализующихся процессов нуклеофильного присоединения атома азота амина к двум карбонильным группам и элиминирования двух молекул воды. Ниже в качестве примера приведена возможная последовательность [136] таких стадий при синтезе 2,5-диметилпиррола [137]:
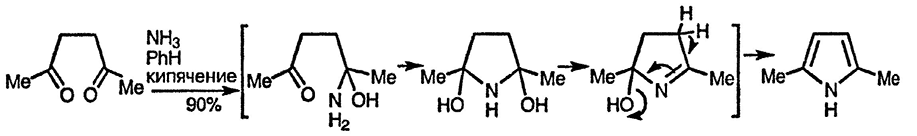
Для синтеза производных пиррола, не содержащих заместителей при атомах углерода, вместо нестабильного янтарного диальдегида используется 2,5-диметокситетрагидрофуран (разд. 15.1.4.) [138] или полученный из него 1,4-дихлор-1,4-диметоксибутан [139]. 2,5-Диметокситетрагидрофуран реагируете алифатическими и ароматическими аминами, эфирами аминокислот, арилсульфонамидами, триметилсилил-этокси-карбонилгидразином [140] и первичными амидами с образованием соответствующих N-замещённых пирролов [141].
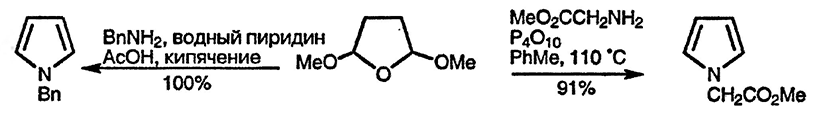
Всё ещё не потерявший своего значения метод получения N-замещённых производных пиррола основан на сухой перегонке алкиламмониевых солей слизевой и сахарной кислот [142] и, вероятно, связан с промежуточным образованием 1,4-дикарбонильных соединений. В целом, процесс проходите высвобождением четырёх молекул воды и двух молекул диоксида углерода и может быть представлен следующей схемой:
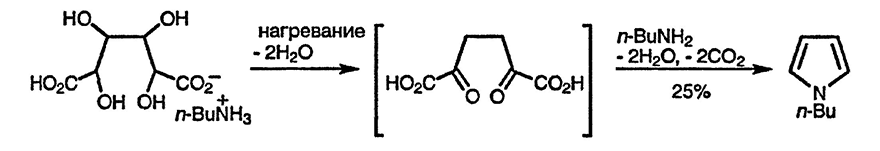
13.18.1.1. Из 1,4-дикарбонильных соединений и аммиака или первичных аминов
Список литературы к главе 13
Упражнения к главе 13
Глава 13
- 13. Пирролы: реакции и методы синтеза
- 13.1. Реакции с электрофильными реагентами
- 13.1.1. Протонирование
- 13.1.1.1. Реакции протонированных пирролов
- 13.1.2. Нитрование
- 13.1.3. Сульфирование и реакции с использованием других серосодержащих электрофильных реагентов
- 13.1.4. Галогенирование
- 13.1.5. Ацилирование
- 13.1.6. Алкилирование
- 13.1.7. Конденсация с альдегидами и кетонами
- 13.1.8. Конденсации с иминами и иминиевыми ионами
- 13.1.9. Сочетание с солями диазония
- 13.2. Реакции с окислителями
- 13.3. Реакции с нуклеофильными реагентами
- 13.4. Реакции с основаниями
- 13.4.1. Депротонирование атома азота
- 13.4.2. Депротонирование по атому углерода
- 13.5. Реакции N-металлированных производных пиррола
- 13.5.1. Литий-, натрий-, калий-, магний- и цинкорганические производные
- 13.6. Реакции C-металлированных производных пиррола
- 13.6.1. Литийорганические производные
- 13.6.2. Реакции, катализируемые палладием
- 13.7. Реакции с радикальными реагентами
- 13.8. Реакции с восстановителями
- 13.9. Электроциклические реакции (основного состояния)
- 13.10. Реакции с карбенами и карбеноидами
- 13.11. Фотохимические реакции
- 13.12. Реакции пиррил-C-X-соединений
- 13.13. Пирролальдегиды и пирролкетоны
- 13.14. Пирролкарбоновые кислоты
- 13.15. Эфиры пирролкарбоновых кислот
- 13.16. Галогенопирролы
- 13.17. Окси- и аминопирролы
- 13.17.1. 2-Оксипирролы
- 13.17.2. 3-Оксипирролы
- 13.17.3. Аминопирролы
- 13.18. Методы синтеза пирролов
- 13.18.1. Синтез кольца
- 13.18.1.1. Из 1,4-дикарбонильных соединений и аммиака или первичных аминов
- 13.18.1.2. Из α-аминокарбонильных соединений и активированных кетонов
- 13.18.1.3. Из α-галогенокарбонильных соединений
- 13.18.1.4. Из тозилметилизоцианида и α,β-непредельных эфиров или кетонов и из изоцианоацетатов и α,β-непредельных нитросоединений
- 13.18.1.5. Из 1,3-дикарбонильных соединений и эфиров глицина
- 13.18.1.6. Из алкинов и оксидооксазолиевых солей
- 13.18.2.1. Некоторые современные общие подходы к синтезу пиррола
- 13.18.2.2. Из альдегидов, аминов и нитроалканов
- 13.18.2.3. Из 4-аминоацетиленов и из 4-аминоацетиленовых кетонов
- 13.18.2.4. Из 2-аминокетонов через промежуточное образование алкилиденкарбенов
- 13.18.3. Примеры синтезов некоторых важных производных пиррола
- 13.18.3.1. Порфобилиноген
- 13.18.3.2. Октаэтилпорфирин
- 13.18.3.3. Октаэтилпорфирин
- 13.18.3.4. Октаэтилгемипорфицен
- 13.18.3.5. Бензо[1,2-b:4,3-b’]дипиррол
- 13.18.3.6. Эпибатидин
Дополнительно:
 Деструкция и стабилизация поливинилхлорида
Деструкция и стабилизация поливинилхлорида В книге изложены вопросы деструкции и стабилизации одного из наиболее ...
 Олигоорганосилоксаны. Свойства, получение, применение
Олигоорганосилоксаны. Свойства, получение, применение В книге рассмотрены физико-химические и эксплуатационные свойства, методы ...
 Общая химия. Состояние веществ и химические реакции
Общая химия. Состояние веществ и химические реакции Рассматриваются многообразные химические реакции, систематизированные по ...