11.14.1.3.3. С использованием галогенозамещённых циклопропенов
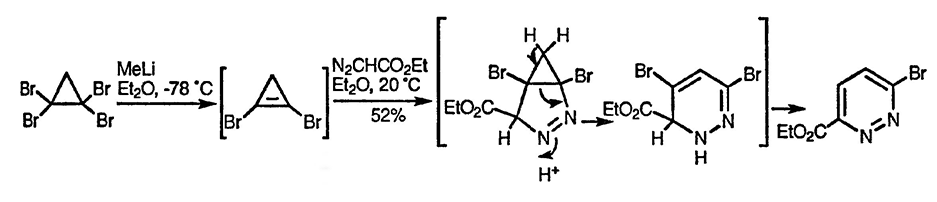
Ди-, три- и тетрагалогенозамещенные циклопропены вступают в реакцию циклоприсоединения с диазоалканами, приводящую к нестабильным пиразолинам, которые легко перегруппировываются в пиридазины с потерей молекулы галогеноводорода. Тетрахлорциклопропен коммерчески доступен, но большинство бромсодержащих производных циклопропена можно синтезировать из винил-бромида в результате двухстадийного синтеза: на первой стадии присоединяется дибромкарбен, а затем циклопропен генерируется in situ при действии метиллития [161]
11.14.1.3.3. С использованием галогенозамещённых циклопропенов
Список литературы к главе 11
Упражнения к главе 11
Глава 11
- 11. Диазины, пиридазины, пиримидины и пиразины: реакции и методы синтеза
- 11.1. Реакции с электрофильными реагентами
- 11.1.1. Присоединение по атому азота
- 11.1.1.1. Протонирование
- 11.1.1.2. Алкилирование
- 11.1.1.3. Окисление
- 11.1.2. Замещение при атоме углерода
- 11.1.2.1. Галогенирование
- 11.2. Реакции с окислителями
- 11.3. Реакции с нуклеофильными реагентами
- 11.3.1. Замещение атома водорода
- 11.3.1.1. Алкилирование и арилирование
- 11.3.1.2. Аминирование
- 11.3.2. Замещение других уходящих групп
- 11.4. Реакции с основаниями
- 11.4.1. Депротонирование при атоме углерода
- 11.4.2. Металлирование
- 11.5. Реакции С-металлированных диазинов
- 11.5.1. Литийорганические производные
- 11.5.2. Реакции, катализируемые палладием
- 11.6. Реакции с восстановителями
- 11.7. Реакции со свободными радикалами
- 11.8. Электроциклические реакции
- 11.9. N-оксиды диазинов
- 11.10. Оксидиазины
- 11.10.1. Строение оксидиазинов
- 11.10.2. Реакции оксидиазинов
- 11.10.2.1. Реакции с электрофильными реагентами
- 11.10.2.2. Реакции с нуклеофильными реагентами
- 11.10.2.3. Реакции с основаниями
- 11.10.2.4. Замещение атома кислорода
- 11.10.2.5. Реакции, катализируемые переходными металлами
- 11.10.2.6. Электроциклические реакции
- 11.11. Аминодиазины
- 11.12. Алкилдиазины
- 11.13. Четвертичные азиниевые соли
- 11.14. Синтез диазинов
- 11.14.1.1. Из 1,4-дикарбонильных соединений и гидразина
- 11.14.1.2. Реакцией циклоприсоединения 1,2,4,5-тетразина к производным ацетилена
- 11.14.1.3. С использованием других реакций циклоприсоединения
- 11.14.1.3.1. С использованием галогеносодержащих гидразонов
- 11.14.1.3.2. С использованием S,S-диоксидов тиофена
- 11.14.1.3.3. С использованием галогенозамещённых циклопропенов
- 11.14.2. Синтез пиримидинового кольца
- 11.14.2.1. Из 1,3-дикарбонильных соединений и соединений, содержащих фрагмент N-C-N
- 11.14.2.2. Реакцией циклоприсоединения 1,3,5-диазинов к производными ацетилена
- 11.14.2.3. Из 3-этоксиакрилоилизоцианата и первичных аминов
- 11.14.3. Синтез пиразинового цикла
- 11.14.3.1. Самоконденсацией 2-аминокетонов
- 11.14.3.2. Из 1,2-дикарбонильных соединений и 1,2-диаминов
- 11.14.3.3. Синтез пиразинов через сульфиды
- 11.14.4. Примеры некоторых важных синтезов диазинов
- 11.14.4.1. 4-Амино-5-циано-2-метилпиримидин
- 11.14.4.2. 4,6-Диамино-5-тиоформамидо-2-метилпиримидин
- 11.14.4.3. Карбоциклический бромвинилдезоксиуридин
- 11.14.4.4. Коелентеразин
- 11.14.4.5. 2,5-Диметил-3-н-пропилпиразин
- 11.15. Птеридины
Дополнительно:
Книги Список книг
 О водном бромокуприте лития
О водном бромокуприте лития Воспроизведено в оригинальной авторской орфографии издания 1898 года ...
 Поверхностно-активные вещества. Синтез, свойства, анализ, применение
Поверхностно-активные вещества. Синтез, свойства, анализ, применение Приведена современная классификация ПАВ и их смесей, рассмотрены технологии ...
 Введение в общую химию
Введение в общую химию Пособие рассматривает отдельные, наиболее сложные аспекты современной химии. ...
 Полуэмпирические методы расчёта электронной структуры (комплект из 2 книг)
Полуэмпирические методы расчёта электронной структуры (комплект из 2 книг) Двухтомная монография из зарубежной серии «Современная теоретическая химия». ...